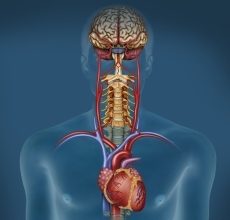
الخلية العصبية: 3 أنواع, ما الفرق بين الخلية العصبية و العصبون؟ النورون العصبي, ما هي وظيفة الخلايا العصبية في الجسم؟ ما الفرق بين الخلية العصبية و العصبون؟ من اين تنشأ الخلايا العصبية؟ متى تنقسم الخلايا العصبية؟ كم عمر الخلايا العصبية؟ كيف تقوي الخلايا العصبية؟ كم عدد أنواع الخلايا العصبية؟ كم عدد الأعصاب في جسم الإنسان؟ كم عدد الخلايا العصبية في جسم الإنسان؟ The Life and Death of a Neuron
الخلايا العصبية
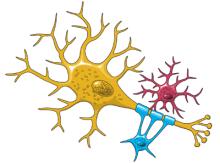
الخلية العصبية هي نفسها العصبون أو neuron
حتى وقت قريب ، اعتقد معظم علماء الأعصاب أننا ولدنا بكل الخلايا العصبية التي كانت لدينا في أي وقت. كأطفال ، قد ننتج بعض الخلايا العصبية الجديدة للمساعدة في بناء المسارات – تسمى الدوائر العصبية – التي تعمل كطرق سريعة للمعلومات بين مناطق مختلفة من الدماغ. لكن العلماء اعتقدوا أنه بمجرد وجود الدائرة العصبية في مكانها ، فإن إضافة أي خلايا عصبية جديدة من شأنه أن يعطل تدفق المعلومات ويعطل نظام الاتصال في الدماغ.
في عام 1962 ، تحدى العالم جوزيف التمان هذا الاعتقاد عندما رأى دليلاً على تكوّن الخلايا العصبية (ولادة الخلايا العصبية) في منطقة من دماغ الفئران البالغة تسمى الحُصين. وذكر لاحقًا أن الخلايا العصبية حديثي الولادة هاجرت من مكان ولادتها في الحُصين إلى أجزاء أخرى من الدماغ. في عام 1979 ، أكد عالم آخر ، مايكل كابلان ، نتائج ألتمان في دماغ الفئران ، وفي عام 1983 وجد خلايا طليعية عصبية في الدماغ الأمامي لقرد بالغ.
كانت هذه الاكتشافات حول تكوين الخلايا العصبية في دماغ البالغين مفاجئة للباحثين الآخرين الذين لم يعتقدوا أنها يمكن أن تكون صحيحة عند البشر. ولكن في أوائل الثمانينيات من القرن الماضي ، اقترح عالم يحاول فهم كيفية تعلم الطيور الغناء أن علماء الأعصاب ينظرون مرة أخرى في تكوين الخلايا العصبية في دماغ البالغين ويبدأون في رؤية كيف يمكن أن يكون ذلك منطقيًا. في سلسلة من التجارب ، أظهر فرناندو نوتيبوم وفريقه البحثي أن عدد الخلايا العصبية في الدماغ الأمامي لذكر طيور الكناري زاد بشكل كبير خلال موسم التزاوج. كان هذا هو الوقت نفسه الذي كان على الطيور أن تتعلم فيه أغاني جديدة لجذب الإناث.
لماذا أضافت أدمغة الطيور هذه الخلايا العصبية في مثل هذا الوقت الحرج من التعلم؟ يعتقد Nottebohm أن السبب هو أن الخلايا العصبية الجديدة ساعدت في تخزين أنماط أغنية جديدة داخل الدوائر العصبية للدماغ الأمامي ، وهي منطقة الدماغ التي تتحكم في السلوكيات المعقدة. جعلت هذه الخلايا العصبية الجديدة التعلم ممكنا. إذا صنعت الطيور خلايا عصبية جديدة لمساعدتها على التذكر والتعلم ، اعتقد نوتيبوم أن أدمغة الثدييات قد تكون كذلك.
يعتقد علماء آخرون أن هذه النتائج لا يمكن أن تنطبق على الثدييات ، لكن إليزابيث جولد وجدت لاحقًا دليلاً على وجود خلايا عصبية حديثي الولادة في منطقة مميزة من الدماغ في القرود ، وأظهر فريد غيج وبيتر إريكسون أن الدماغ البشري البالغ ينتج خلايا عصبية جديدة في منطقة مماثلة.
بالنسبة لبعض علماء الأعصاب ، لا يزال تكوين الخلايا العصبية في دماغ البالغين نظرية غير مثبتة. لكن يعتقد البعض الآخر أن الأدلة تقدم احتمالات مثيرة للاهتمام حول دور الخلايا العصبية التي يولدها البالغون في التعلم والذاكرة.

تركيب وبنية العصبون:
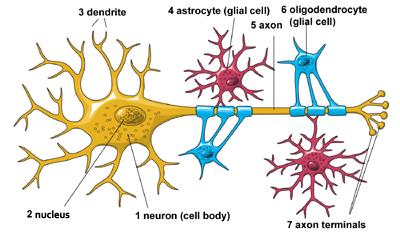
يتكون الجهاز العصبي المركزي (الذي يشمل الدماغ والنخاع الشوكي) من نوعين أساسيين من الخلايا: الخلايا العصبية (1) والدبقية (4) و (6). يفوق عدد الخلايا الدبقية عدد الخلايا العصبية في بعض أجزاء الدماغ ، لكن الخلايا العصبية هي اللاعب الرئيسي في الدماغ.
الخلايا العصبية هي رسل معلومات. يستخدمون النبضات الكهربائية والإشارات الكيميائية لنقل المعلومات بين مناطق مختلفة من الدماغ ، وبين الدماغ وبقية الجهاز العصبي. كل شيء نفكر فيه ونشعر به ونفعله سيكون مستحيلًا بدون عمل الخلايا العصبية والخلايا الداعمة لها ، الخلايا الدبقية المسماة الخلايا النجمية (4) والخلايا الدبقية قليلة التغصن (6).
تتكون الخلايا العصبية من ثلاثة أجزاء أساسية: جسم الخلية وامتدادان يسمىان محور عصبي (5) وتغصنات (3). يوجد داخل جسم الخلية نواة (2) تتحكم في أنشطة الخلية وتحتوي على المادة الوراثية للخلية. يشبه المحوار ذيلًا طويلًا وينقل الرسائل من الخلية. تبدو التشعبات مثل فروع شجرة وتتلقى رسائل للخلية. تتواصل الخلايا العصبية مع بعضها البعض عن طريق إرسال مواد كيميائية ، تسمى الناقلات العصبية ، عبر مساحة صغيرة ، تسمى المشبك ، بين المحاور والتشعبات للخلايا العصبية المجاورة.
هناك ثلاث فئات من الخلايا العصبية:
- تحمل الخلايا العصبية الحسية المعلومات من أعضاء الحس (مثل العينين والأذنين) إلى الدماغ.
- تتحكم الخلايا العصبية الحركية في نشاط العضلات الإرادي مثل التحدث ونقل الرسائل من الخلايا العصبية في الدماغ إلى العضلات.
- جميع الخلايا العصبية الأخرى تسمى interneurons .
يعتقد العلماء أن الخلايا العصبية هي أكثر أنواع الخلايا تنوعًا في الجسم. يوجد ضمن هذه الفئات الثلاث من الخلايا العصبية مئات الأنواع المختلفة ، ولكل منها قدرات محددة في حمل الرسائل.
كيف تتواصل هذه الخلايا العصبية مع بعضها البعض عن طريق تكوين روابط هو ما يجعل كل واحد منا فريدًا في طريقة تفكيرنا وشعورنا وتصرفنا.
ولادة او تكون الخلايا العصبية:
يعد مدى توليد الخلايا العصبية الجديدة في الدماغ موضوعًا مثيرًا للجدل بين علماء الأعصاب. على الرغم من أن غالبية الخلايا العصبية موجودة بالفعل في أدمغتنا بحلول الوقت الذي نولد فيه ، إلا أن هناك أدلة تدعم أن تكون الخلايا العصبية (الكلمة العلمية لولادة الخلايا العصبية) هي عملية تستمر مدى الحياة.
تولد الخلايا العصبية في مناطق من الدماغ غنية بتركيزات الخلايا العصبية الأولية (وتسمى أيضًا الخلايا الجذعية العصبية). تمتلك هذه الخلايا القدرة على إنتاج معظم ، إن لم يكن كل ، الأنواع المختلفة من الخلايا العصبية والدبقية الموجودة في الدماغ.
لاحظ علماء الأعصاب كيف تتصرف الخلايا السليفة العصبية في المختبر. على الرغم من أن هذا قد لا يكون بالضبط كيف تتصرف هذه الخلايا عندما تكون في الدماغ ، إلا أنها تعطينا معلومات حول كيف يمكن أن تتصرف عندما تكون في بيئة الدماغ.
لا يزال علم الخلايا الجذعية جديدًا جدًا ، ويمكن أن يتغير مع اكتشافات إضافية ، لكن الباحثين تعلموا ما يكفي ليكونوا قادرين على وصف كيفية توليد الخلايا الجذعية العصبية لخلايا الدماغ الأخرى. يسمونه سلالة الخلايا الجذعية وهو مشابه من حيث المبدأ لشجرة العائلة.
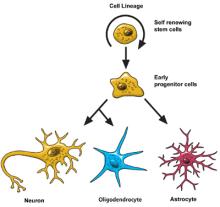
تزداد الخلايا الجذعية العصبية عن طريق الانقسام إلى خليتين وإنتاج خليتين جذعتين جديدتين ، أو خليتين سلف مبكرتين ، أو خلية واحدة من كل منهما.
عندما تنقسم خلية جذعية لإنتاج خلية جذعية أخرى ، يُقال إنها تتجدد ذاتيًا. هذه الخلية الجديدة لديها القدرة على إنتاج المزيد من الخلايا الجذعية.
عندما تنقسم الخلية الجذعية لإنتاج خلية سلفية مبكرة ، يُقال إنها تتمايز. التمايز يعني أن الخلية الجديدة أكثر تخصصًا في الشكل والوظيفة. لا تتمتع الخلية السلفية المبكرة بإمكانية الخلية الجذعية لتكوين العديد من أنواع الخلايا المختلفة. يمكنه فقط تكوين خلايا في سلالته الخاصة.
يمكن للخلايا السلفية المبكرة أن تتجدد ذاتيًا أو تتجدد بإحدى الطريقتين. نوع واحد سوف يؤدي إلى ظهور الخلايا النجمية. النوع الآخر سينتج في النهاية الخلايا العصبية أو الخلايا الدبقية قليلة التغصن.
الهجرة :
بمجرد أن يولد أي خلية عصبية ، عليها أن تنتقل إلى مكان في الدماغ حيث ستقوم بعملها.
كيف يعرف العصبون إلى أين يذهب؟ ما الذي يساعدها للوصول إلى هناك؟
لاحظ العلماء أن الخلايا العصبية تستخدم طريقتين مختلفتين على الأقل للسفر:
- تهاجر بعض الخلايا العصبية باتباع ألياف طويلة من الخلايا تسمى الدبقية الشعاعية. تمتد هذه الألياف من الطبقات الداخلية إلى الطبقات الخارجية للدماغ. تنزلق الخلايا العصبية على طول الألياف حتى تصل إلى وجهتها.
- تنتقل الخلايا العصبية أيضًا باستخدام الإشارات الكيميائية. وجد العلماء جزيئات خاصة على سطح الخلايا العصبية – جزيئات الالتصاق – ترتبط بجزيئات مماثلة على الخلايا الدبقية القريبة أو محاور الأعصاب. توجه هذه الإشارات الكيميائية العصبون إلى موقعه النهائي.
ليست كل الخلايا العصبية ناجحة في رحلتهم. يعتقد العلماء أن ثلثهم فقط يصل إلى وجهتهم. تموت بعض الخلايا أثناء عملية نمو الخلايا العصبية.
تنجو بعض الخلايا العصبية من الرحلة ، لكن ينتهي بها الأمر حيث لا ينبغي أن تكون. الطفرات في الجينات التي تتحكم في الهجرة تخلق مناطق من الخلايا العصبية في غير محلها أو تكونت بشكل غريب والتي يمكن أن تسبب اضطرابات مثل صرع الطفولة. يشك بعض الباحثين في أن الفصام واضطراب التعلم عسر القراءة هما نتيجة جزئية للخلايا العصبية المضللة.

التفاضل او تمايز الخلايا العصبية:
بمجرد أن تصل الخلية العصبية إلى وجهتها ، يجب أن تستقر لتعمل. هذه الخطوة الأخيرة من التمايز هي الجزء الأقل فهماً من تكوين الخلايا العصبية.
الخلايا العصبية مسؤولة عن نقل وامتصاص النواقل العصبية – المواد الكيميائية التي تنقل المعلومات بين خلايا الدماغ.
اعتمادًا على موقعها ، يمكن للخلايا العصبية أداء وظيفة الخلايا العصبية الحسية أو الخلايا العصبية الحركية أو الخلايا العصبية الداخلية ، وإرسال واستقبال نواقل عصبية محددة.
في الدماغ النامي ، تعتمد الخلية العصبية على الإشارات الجزيئية من الخلايا الأخرى ، مثل الخلايا النجمية ، لتحديد شكلها وموقعها ، ونوع المرسل الذي تنتجه ، والخلايا العصبية الأخرى التي ستتصل بها. تنشئ هذه الخلايا المولودة حديثًا دوائر عصبية – أو مسارات معلومات تربط الخلايا العصبية بالخلايا العصبية – والتي ستكون في مكانها طوال فترة البلوغ.
ولكن في دماغ البالغين ، تم تطوير الدوائر العصبية بالفعل ويجب أن تجد الخلايا العصبية طريقة لتلائمها. وعندما تستقر خلية عصبية جديدة ، تبدأ في الظهور مثل الخلايا المحيطة. يطور محور عصبي وتغصنات ويبدأ في التواصل مع جيرانه.
موت الخلية العصبية:
على الرغم من أن الخلايا العصبية هي أطول الخلايا الحية في الجسم ، إلا أن أعدادًا كبيرة منها تموت أثناء الهجرة والتمايز.
يمكن أن تأخذ حياة بعض الخلايا العصبية منعطفات غير طبيعية. تحدث بعض أمراض الدماغ نتيجة الموت غير الطبيعي للخلايا العصبية.
- في مرض باركنسون ، تموت الخلايا العصبية التي تفرز الناقل العصبي الدوبامين في العقد القاعدية ، وهي منطقة من الدماغ تتحكم في حركات الجسم. هذا يسبب صعوبة في بدء الحركة.
- في مرض هنتنغتون ، تتسبب طفرة جينية في زيادة إنتاج ناقل عصبي يسمى الغلوتامات ، والذي يقتل الخلايا العصبية في العقد القاعدية. نتيجة لذلك ، يلتف الناس ويلتفون دون حسيب ولا رقيب.
- في مرض الزهايمر ، تتراكم بروتينات غير معتادة في الخلايا العصبية وحولها في القشرة المخية الحديثة والحصين ، وهي أجزاء من الدماغ تتحكم في الذاكرة. عندما تموت هذه الخلايا العصبية ، يفقد الناس قدرتهم على التذكر وقدرتهم على أداء المهام اليومية. يمكن للضرر الجسدي الذي يصيب الدماغ وأجزاء أخرى من الجهاز العصبي المركزي أن يقتل أو يعطل الخلايا العصبية.
- يمكن للضربات في الدماغ ، أو الضرر الناجم عن السكتة الدماغية ، أن تقتل الخلايا العصبية تمامًا أو تجويعها ببطء من الأكسجين والمواد المغذية التي تحتاجها للبقاء على قيد الحياة.
- يمكن أن تؤدي إصابة الحبل الشوكي إلى تعطيل الاتصال بين الدماغ والعضلات عندما تفقد الخلايا العصبية اتصالها بالمحاور الموجودة أسفل موقع الإصابة. قد تظل هذه الخلايا العصبية حية ، لكنها تفقد قدرتها على التواصل.
الأمل من خلال البحث:
يأمل العلماء أنه من خلال فهم المزيد عن حياة الخلايا العصبية وموتها ، يمكنهم تطوير علاجات جديدة ، وربما حتى علاج ، لأمراض واضطرابات الدماغ التي تؤثر على حياة ملايين الأمريكيين.
تشير أحدث الأبحاث إلى أن الخلايا الجذعية العصبية يمكن أن تولد العديد من الأنواع المختلفة من الخلايا العصبية الموجودة في الدماغ والجهاز العصبي ، إن لم يكن كلها. تعلم كيفية التعامل مع هذه الخلايا الجذعية في المختبر إلى أنواع معينة من الخلايا العصبية يمكن أن ينتج إمدادات جديدة من خلايا الدماغ لتحل محل تلك التي ماتت أو تضررت.
يمكن أيضًا إنشاء علاجات للاستفادة من عوامل النمو وآليات الإشارات الأخرى داخل الدماغ التي تخبر الخلايا السليفة بتكوين خلايا عصبية جديدة. هذا من شأنه أن يجعل من الممكن إصلاح وإعادة تشكيل وتجديد الدماغ من الداخل.
الجينات والدماغ
تقوم الجينات بأكثر من مجرد تحديد لون أعيننا أو ما إذا كنا طويلين أو قصيري القامة. الجينات هي مركز كل ما يجعلنا بشر.
الجينات مسؤولة عن إنتاج البروتينات التي تدير كل شيء في أجسامنا. بعض البروتينات مرئية ، مثل تلك التي يتكون منها شعرنا وجلدنا. يعمل آخرون بعيدًا عن الأنظار ، وينسقون وظائفنا البيولوجية الأساسية.
بالنسبة للجزء الأكبر ، تحتوي كل خلية في أجسامنا على نفس الجينات تمامًا ، ولكن داخل الخلايا الفردية ، تنشط بعض الجينات بينما لا ينشط البعض الآخر. عندما تنشط الجينات ، تكون قادرة على إنتاج البروتينات. هذه العملية تسمى التعبير الجيني. عندما تكون الجينات غير نشطة ، فإنها تكون صامتة أو يتعذر الوصول إليها لإنتاج البروتين.
ما لا يقل عن ثلث ما يقرب من 20000 جينة مختلفة التي تتكون منها الجينوم البشري نشطة (معبرة) بشكل أساسي في الدماغ. هذه هي أعلى نسبة من الجينات يتم التعبير عنها في أي جزء من الجسم. تؤثر هذه الجينات على تطور ووظيفة الدماغ ، وتتحكم في النهاية في كيفية تحركنا وتفكيرنا وشعورنا وتصرفنا. بالاقتران مع تأثيرات بيئتنا ، يمكن للتغييرات في هذه الجينات أن تحدد أيضًا ما إذا كنا معرضين لخطر الإصابة بمرض معين ، وإذا كنا كذلك ، فالمسار الذي قد يتبعه.
هذا الكتيب هو مقدمة عن الجينات ، وكيف تعمل في الدماغ ، وكيف تساعد الأبحاث الجينية في الوصول إلى علاجات جديدة للاضطرابات العصبية.
من الحمض النووي
من أجل فهم كيفية عمل الجينات في الدماغ ، علينا أن نفهم كيف تصنع الجينات البروتينات. يبدأ هذا بالحمض النووي (الحمض النووي الريبي منقوص الأكسجين).
الحمض النووي هو جزيء طويل معبأ في هياكل تسمى الكروموسومات. لدى البشر 23 زوجًا من الكروموسومات ، بما في ذلك زوج واحد من الكروموسومات الجنسية (XX في الإناث و XY في الذكور). داخل كل زوج ، يأتي كروموسوم واحد من أم الفرد والآخر يأتي من الأب. بعبارة أخرى ، نحن نرث نصف حمضنا النووي من كل من والدينا.
يتكون الحمض النووي من خيطين ملفوفين معًا لتشكيل حلزون مزدوج. داخل كل خيط ، يتم استخدام مواد كيميائية تسمى النيوكليوتيدات كرمز لصنع البروتينات. يحتوي الحمض النووي على أربعة نيوكليوتيدات فقط – الأدينين (A) ، والثايمين (T) ، والسيتوزين (C) ، والجوانين (G) – ولكن هذه الأبجدية الجينية البسيطة هي نقطة البداية لصنع جميع البروتينات في جسم الإنسان ، والتي يُقدر أنها ما يصل إلى مليون.
إلى الجين
الجين هو امتداد للحمض النووي يحتوي على تعليمات لصنع بروتين معين أو تنظيمه.
تسمى الجينات التي تصنع البروتينات جينات ترميز البروتين. من أجل صنع بروتين ، يقوم جزيء وثيق الصلة بالحمض النووي يسمى الحمض النووي الريبي (RNA) أولاً بنسخ الشفرة داخل الحمض النووي. بعد ذلك ، تقوم آلات تصنيع البروتين داخل الخلية بمسح الحمض النووي الريبي ، وقراءة النيوكليوتيدات في مجموعات من ثلاثة. تقوم هذه الثلاثيات بترميز 20 من الأحماض الأمينية المتميزة ، والتي تعد اللبنات الأساسية للبروتينات. أكبر بروتين بشري معروف هو بروتين عضلي يسمى تيتين ، والذي يتكون من حوالي 27000 من الأحماض الأمينية.
تقوم بعض الجينات بترميز أجزاء صغيرة من الحمض النووي الريبي (RNA) التي لا تُستخدم في صنع البروتينات ، ولكنها تُستخدم بدلاً من ذلك لإخبار البروتينات بما يجب أن تفعله وأين تذهب. وتسمى هذه الجينات غير المشفرة أو الجينات RNA. يوجد العديد من جينات RNA أكثر من جينات ترميز البروتين.
البروتين
تشكل البروتينات الآلية الداخلية داخل خلايا الدماغ والنسيج الضام بين خلايا الدماغ. كما أنها تتحكم في التفاعلات الكيميائية التي تسمح لخلايا الدماغ بالتواصل مع بعضها البعض.
تصنع بعض الجينات بروتينات مهمة للتطور المبكر والنمو لدماغ الرضيع. على سبيل المثال ، يصنع جين ASPM بروتينًا ضروريًا لإنتاج خلايا عصبية جديدة (أو خلايا عصبية) في الدماغ النامي. يمكن أن تؤدي التعديلات في هذا الجين إلى صغر الرأس ، وهي حالة يفشل فيها الدماغ في النمو إلى حجمه الطبيعي.
تصنع جينات معينة بروتينات تصنع بدورها نواقل عصبية ، وهي مواد كيميائية تنقل المعلومات من خلية عصبية إلى أخرى. البروتينات الأخرى مهمة لإنشاء اتصالات فيزيائية تربط الخلايا العصبية المختلفة معًا في الشبكات.
لا تزال جينات أخرى تصنع بروتينات تعمل كمدبرة منزل في الدماغ ، وتحافظ على الخلايا العصبية وشبكاتها في حالة عمل جيدة.
على سبيل المثال ، يصنع جين SOD1 بروتينًا يحارب تلف الحمض النووي في الخلايا العصبية. تعد التعديلات في هذا الجين أحد أسباب مرض التصلب الجانبي الضموري (ALS) ، حيث يؤدي الفقد التدريجي للخلايا العصبية التي تتحكم في العضلات إلى الشلل والموت في نهاية المطاف. يُعتقد أن جين SOD1 يحمل أدلة مهمة حول سبب موت الخلايا العصبية في الشكل “المتقطع” الشائع لـ ALS ، والذي ليس له سبب معروف.
كيف يتم تنظيم التعبير الجيني
نحن نعرف أي بروتين سيصنعه الجين من خلال النظر إلى شفرته ، وتسمى أيضًا تسلسل الحمض النووي الخاص به. ما لا يمكننا التنبؤ به هو كمية البروتين التي سيتم تصنيعها ، ومتى سيتم تصنيعها ، أو ما هي الخلية التي ستصنعها.
تقوم كل خلية بتشغيل جزء بسيط فقط من جيناتها ، بينما تقوم بإسكات الباقي. على سبيل المثال ، قد يتم إسكات الجينات التي يتم التعبير عنها في خلايا الدماغ في خلايا الكبد أو خلايا القلب. يتم تشغيل بعض الجينات فقط خلال الأشهر الأولى من التطور البشري ثم يتم إسكاتها لاحقًا.
ما الذي يحدد هذه الأنماط الفريدة للتعبير الجيني؟ الخلايا لها سلالة فريدة مثل البشر ، وتميل إلى وراثة الصفات من والديها. لذلك ، تؤثر أصول الخلية على الجينات التي تقوم بتشغيلها لإنتاج البروتينات. تساعد بيئة الخلية – تعرضها للخلايا المحيطة وللهرمونات والإشارات الأخرى – أيضًا على تحديد البروتينات التي تصنعها الخلية. تعمل هذه الإشارات من ماضي الخلية ومن بيئتها من خلال العديد من العوامل التنظيمية داخل الخلية ، وبعضها موصوف في الأقسام التالية.
- بروتينات ربط الحمض النووي:
حوالي 10 بالمائة من الجينات في الجينوم البشري تقوم بتشفير بروتينات ربط الحمض النووي. تتعرف بعض هذه البروتينات على أجزاء معينة من الحمض النووي وترتبط بها لتنشيط التعبير الجيني. نوع آخر من بروتين ربط الحمض النووي ، يسمى هيستون ، يعمل كبكرة يمكنها الحفاظ على الحمض النووي في ملفات ضيقة وبالتالي قمع التعبير الجيني. - توجد أنواع عديدة من الحمض النووي
الريبي الصغير (sRNA) المنتشرة في جميع أنحاء الجينوم والتي تنظم بشكل فعال التعبير الجيني. نظرًا لقصر طولها ، فإنها قادرة على استهداف ، ومطابقة ، وإلغاء تنشيط أجزاء صغيرة من الشفرة الجينية. - العوامل اللاجينية
تأتي كلمة علم التخلق من الكلمة اليونانية epi ، والتي تعني أعلاه أو بجانب. بمعنى واسع ، يشير علم التخلق إلى تغييرات طويلة الأمد في التعبير الجيني دون أي تغييرات في الكود الجيني. تشمل العوامل الوراثية اللاجينية العلامات أو العلامات الكيميائية الموجودة على الحمض النووي أو الهستونات التي يمكن أن تؤثر على التعبير الجيني.
الاختلافات في الكود الجيني
الاختلاف الجيني هو تغيير دائم في تسلسل الحمض النووي الذي يتكون من الجين. معظم الاختلافات غير ضارة أو ليس لها تأثير على الإطلاق. ومع ذلك ، يمكن أن يكون للاختلافات الأخرى آثار ضارة تؤدي إلى المرض. لا يزال البعض الآخر مفيدًا على المدى الطويل ، مما يساعد الأنواع على التكيف مع التغيير.
تعدد أشكال النوكليوتيدات الأحادية (SNP)
هي أشكال متنوعة تتضمن تغييرًا في نيوكليوتيد واحد فقط. تشير التقديرات إلى أن الجينوم البشري يحتوي على أكثر من 10 ملايين تعدد الأشكال المختلفة. نظرًا لأن SNPs عبارة عن تغييرات صغيرة داخل الحمض النووي ، فإن معظمها ليس له أي تأثير على التعبير الجيني. ومع ذلك ، فإن بعض أشكال النيوكلوتايد مسئولة عن منحنا سمات فريدة ، مثل لون الشعر والعين. قد يكون لأشكال النيوكلوتايد الأخرى تأثيرات طفيفة على خطر الإصابة بأمراض شائعة ، مثل أمراض القلب أو السكري أو السكتة الدماغية.
تباين رقم النسخ (CNV)
يتكون ما لا يقل عن 10 بالمائة من الجينوم البشري من CNVs ، وهي أجزاء كبيرة من الحمض النووي يتم حذفها أو نسخها أو قلبها أو إعادة ترتيبها في مجموعات يمكن أن تكون فريدة لكل فرد. غالبًا ما تشتمل هذه القطع من الحمض النووي على جينات مشفرة للبروتين. هذا يعني أنه من المحتمل أن تغير CNVs الطريقة التي يصنع بها الجين بروتينه.
نظرًا لأن الجينات تحدث عادةً في نسختين ، واحدة موروثة من كل والد ، فإن CNV الذي يتضمن جينًا واحدًا مفقودًا يمكن أن يقلل من إنتاج البروتين أقل من الكمية المطلوبة.
قد يكون وجود عدد كبير جدًا من نسخ الجين ضارًا أيضًا. على الرغم من أن معظم حالات مرض باركنسون متقطعة (بدون سبب معروف) ، فقد تم ربط بعض الحالات بامتلاك نسختين أو أكثر من جين SNCA ، الذي يشفر بروتينًا يسمى ألفا سينوكلين. يتراكم ألفا سينوكلين الزائد في كتل داخل خلايا الدماغ ، ويبدو أنه يعيق آلية الخلايا. لأسباب غير واضحة ، ترتبط الكتل المتشابهة بمرض باركنسون المتقطع.
طفرة الجين الفردي
بعض الاختلافات الجينية صغيرة وتؤثر على جين واحد فقط. يمكن أن يكون لهذه الطفرات الجينية المفردة عواقب وخيمة ، لأنها تؤثر على تعليمات الجين لصنع البروتين. تعد الطفرات الجينية المنفردة مسؤولة عن العديد من الأمراض العصبية الموروثة النادرة.
على سبيل المثال ، مرض هنتنغتون هو نتيجة لما يسمى “التكرار الثلاثي الموسع” في جين هنتنغتين. غالبًا ما تحتوي الجينات الطبيعية على تكرارات ثلاثية ، حيث يحدث نفس رمز الحمض الأميني الثلاثي عدة مرات مثل التلعثم. عادة ما تكون هذه التكرارات غير ضارة.
في جين هنتنغتين ، تكون التكرارات الثلاثية من 20 إلى 30 مرة طبيعية. ولكن في الأشخاص المصابين بمرض هنتنغتون ، يصل عدد مرات التكرار إلى 40 أو أكثر. تخلق الطفرة بروتينًا غير طبيعي الشكل يكون سامًا للخلايا العصبية. عندما تبدأ الخلايا في الموت ، تظهر أعراض مرض هنتنغتون – حركات ملتوية لا يمكن السيطرة عليها في الساقين والذراعين ، وفقدان التنسيق العضلي ، وتغيرات في الشخصية والتفكير.
دور الجينات في الأمراض العصبية
تم تحديد معظم الطفرات الجينية التي تسبب اضطرابات عصبية نادرة مثل مرض هنتنغتون. في المقابل ، لا يزال هناك الكثير لنتعلمه عن دور الاختلافات الجينية في الاضطرابات والحالات العصبية الشائعة ، مثل مرض الزهايمر والسكتة الدماغية. بعض الأشياء واضحة. أولاً ، بالنسبة لمعظم الناس ، يؤثر التفاعل المعقد بين الجينات والبيئة على خطر الإصابة بهذه الأمراض. ثانيًا ، عندما يكون من المعروف أن الاختلافات الجينية المحددة مثل الأشكال المتعددة للنماذج المتعددة الأشكال تؤثر على مخاطر الإصابة بالأمراض ، فإن تأثير أي اختلاف فردي يكون عادةً صغيرًا جدًا. بعبارة أخرى ، يعاني معظم الأشخاص المصابين بالسكتة الدماغية أو مرض الزهايمر من مزيج مؤسف من العديد من “الضربات” في الجينوم وفي البيئة. أخيرًا ، بعد التغييرات في تسلسل الحمض النووي ، التغييرات في تنظيم الجينات – على سبيل المثال ،
يبحث العلماء عن الروابط بين الجينات ومخاطر الأمراض من خلال إجراء نوعين من الدراسات. في دراسة الارتباط على مستوى الجينوم (GWA) ، يبحث العلماء عن SNPs أو تغييرات أخرى في تسلسل الحمض النووي ، ومقارنة جينومات الأشخاص (الأشخاص أو حيوانات المختبر أو الخلايا) التي لديها مرض والموضوعات التي لا تعاني من المرض. في نوع آخر من الدراسات يسمى تحديد ملامح التعبير الجيني ، يبحث العلماء عن التغييرات في التعبير الجيني والتنظيم المرتبط بالمرض.
غالبًا ما يستخدم كلا النوعين من الدراسات جهازًا يسمى ميكروأري DNA ، وهو عبارة عن شريحة صغيرة ، تسمى أحيانًا شريحة جينية ، مغلفة بصف تلو صف من شظايا الحمض النووي. تعمل الشظايا كمجسات للحمض النووي (في دراسة GWA) أو الحمض النووي الريبي (في تحديد ملامح التعبير الجيني) المعزولة من عينة من الدم أو الأنسجة.
يقوم العلماء على نحو متزايد بإجراء هذه الدراسات عن طريق التسلسل المباشر ، والذي يتضمن قراءة تسلسل الحمض النووي أو الحمض النووي الريبي للنيوكليوتيدات بواسطة النيوكليوتيدات. كان التسلسل إجراءً مستهلكًا للوقت ومكلفًا ، ولكن ظهرت مجموعة جديدة من التقنيات تسمى تسلسل الجيل التالي كطريقة فعالة وفعالة من حيث التكلفة للحصول على قراءة مفصلة للجينوم.

الجينات في العمل من أجل علاج وعلاج أفضل
يمكن للأطباء وصف الاختبارات القائمة على الحمض النووي للبحث عن الطفرات التي تسبب اضطرابات طفرة جينية واحدة مثل الحثل العضلي الدوشيني ، والورم الليفي العصبي من النوع الأول ، ومرض هنتنغتون. غالبًا ما تُستخدم الاختبارات الجينية لتأكيد تشخيص المرض لدى الأشخاص الذين لديهم أعراض بالفعل ، ولكن يمكن أيضًا استخدامها لإثبات وجود طفرة لدى الأفراد المعرضين لخطر الإصابة بالمرض ولكنهم لم تظهر عليهم أي أعراض بعد.
في المختبر ، تؤدي دراسات GWA ودراسات تحديد ملامح التعبير الجيني إلى رؤى حول إمكانيات جديدة للوقاية من الأمراض وتشخيصها وعلاجها. عندما يحدد العلماء المسار التنظيمي للجين أو الجين المرتبط بمرض ما ، فإنهم يكشفون عن أهداف جديدة محتملة للعلاج.
من المتوقع أيضًا أن يلعب فهم العلاقات بين الجينات والأمراض المعقدة دورًا مهمًا في الطب الشخصي. في يوم من الأيام ، يمكن أن يصبح مسح الجينوم المستند إلى المصفوفات الدقيقة طريقة روتينية لتقدير الخطر الوراثي للإصابة بأمراض مثل السكتة الدماغية ومرض الزهايمر ومرض باركنسون وبعض أنواع سرطانات الدماغ. يأمل الباحثون أيضًا في تطوير “كوكتيلات” مخصّصة للأدوية تتوافق مع الخصائص الجينية الفريدة للشخص. يعتقد الباحثون أن هذه الأدوية المخصصة ستكون أقل احتمالا بكثير من الأدوية الحالية للتسبب في آثار جانبية.
تداخل RNA (RNAi) هي تقنية تستفيد من قدرة RNAs الصغيرة على تعديل التعبير الجيني. في المستقبل ، يمكن استخدام RNAi علاجيًا لتشغيل الجين الذي تم إسكاته بشكل غير طبيعي ، أو لإيقاف الجين المفرط النشاط. لا يزال هناك العديد من العقبات التقنية التي يجب التغلب عليها قبل أن تصبح هذه الأنواع من العلاجات حقيقة واقعة. على سبيل المثال ، لا يعرف الباحثون بعد أفضل طريقة لإيصال هذه الجزيئات إلى الجهاز العصبي.
هذه ليست سوى عدد قليل من الطرق التي يستخدم بها العلماء المعرفة المكتشفة حديثًا حول التعبير الجيني لجعل الحياة أفضل للأشخاص الذين يعانون من اضطرابات عصبية.
آخر تحديث: 18/02/2023- المصدر: .ninds.nih.gov