تحليل البروكالسيتونين
ما هو تحليل PCT, ما هو المعدل الطبيعي PCT؟ ما هو الغرض من اختبار الدم PCT؟ ما هي أسباب ارتفاع مستوى البروكالسيتونين بخلاف الإنتان؟
التفاصيل فيما يلي:
مقدمة حول تحليل البروكالسيتونين:
في الممارسة السريرية الحالية، برز البروكالسيتونين (PCT) كعلامة حيوية واعدة للكشف المبكر عن العدوى البكتيرية الجهازية. يتكون البروكالسيتونين من 116 حمضًا أمينيًا، وقد وصفه لو موليك وزملاؤه لأول مرة عام 1984، إلا أن أهميته التشخيصية لم تُعرف إلا عام 1993. [1] في عام 1993، أثبت أسيكوت وزملاؤه وجود ارتباط إيجابي بين ارتفاع مستويات البروكالسيتونين في الدم ووجود نتائج إيجابية للعدوى البكتيرية والإنتان (مثل نتائج إيجابية لزراعة الدم). كما أثبتوا أن البروكالسيتونين لا يرتفع في حالات العدوى الفيروسية، وأن مستوياته في الدم تنخفض بعد إعطاء المضادات الحيوية المناسبة. [2]
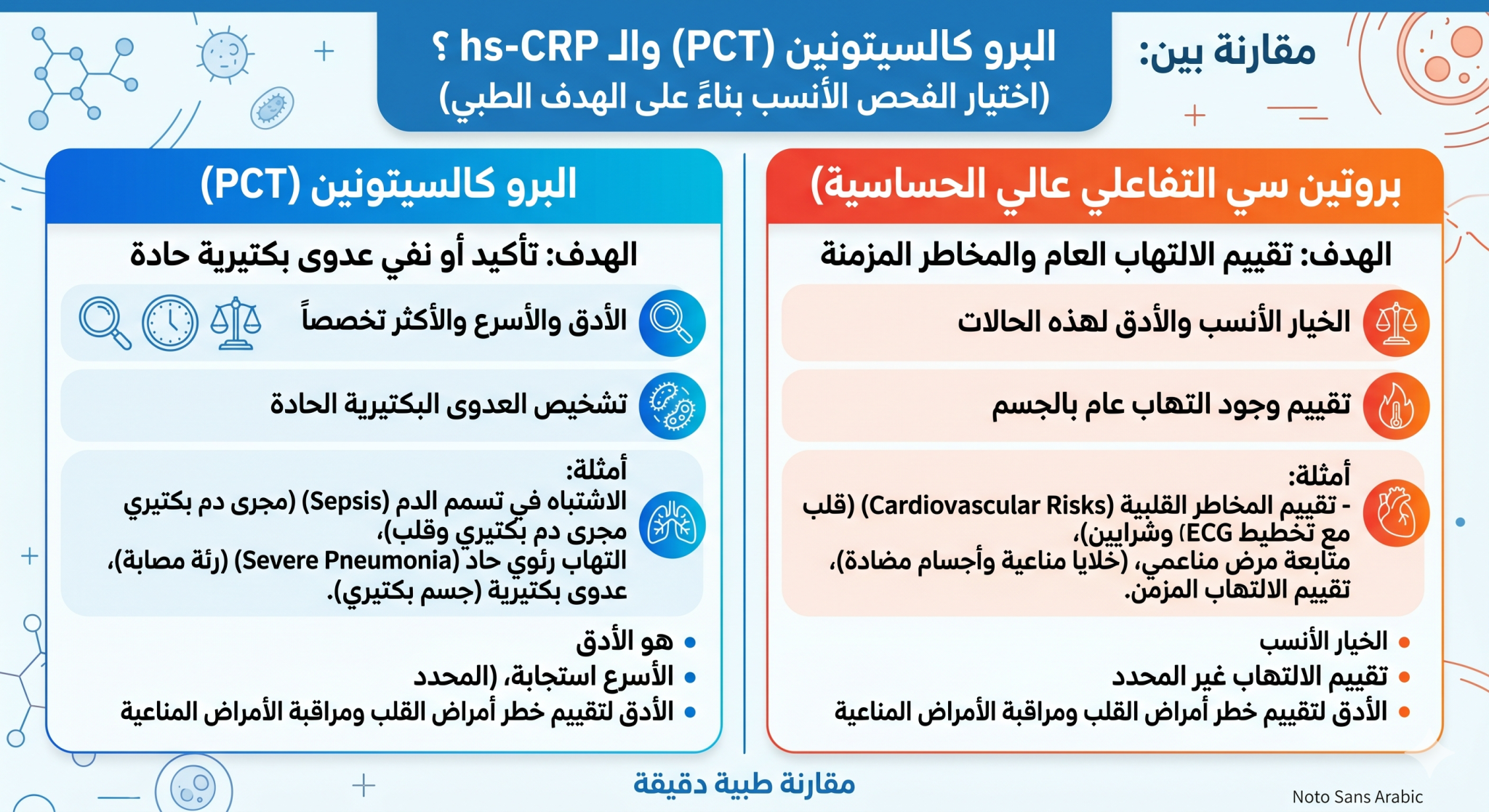
تفتقر المؤشرات الحيوية الالتهابية الأخرى، مثل البروتين المتفاعل C، إلى الخصوصية اللازمة للتمييز بدقة بين العدوى البكتيرية وغير البكتيرية. [3] لذلك، تم تطوير فحوصات البروكالسيتونين (PCT)، التي تتميز بخصوصية تبلغ 79%، واستخدامها لتحديد ما إذا كان التفاعل الالتهابي الجهازي ناتجًا عن نوع من البكتيريا بدقة أكبر. [4]
وافقت إدارة الغذاء والدواء الأمريكية على استخدام اختبارات البروكالسيتونين (PCT) لبدء أو إيقاف المضادات الحيوية في حالات التهابات الجهاز التنفسي السفلي، وكذلك لإيقافها لدى مرضى الإنتان. [5] وقد قيّمت دراسات عديدة خوارزميات العلاج القائمة على اختبار البروكالسيتونين في هذه الحالات، ووجدت أنها آمنة مقارنةً بالرعاية القياسية. [6] وعلى وجه الخصوص، يسمح استخدام اختبارات البروكالسيتونين بإيقاف العلاج بالمضادات الحيوية دون زيادة في معدلات الاعتلال والوفيات. وهذا ما يجعل اختبار البروكالسيتونين أداةً مفيدةً محتملةً للوقاية من ظهور الكائنات المقاومة للمضادات الحيوية، مع ضمان استمرار العلاج المناسب للعدوى البكتيرية الخطيرة. [4]
لا ينبغي استخدام اختبار البروكالسيتونين (PCT) كمعيار وحيد لتحديد العلاج بالمضادات الحيوية. [7] يجب وضع نتائج اختبار البروكالسيتونين في سياق الحالة السريرية مع مراعاة الموقع المحتمل للعدوى، واحتمالية الإصابة بعدوى بكتيرية، وشدة المرض، وغيرها من البيانات السريرية ذات الصلة. [8]
الفيزيولوجيا المرضية لتحليل البروكالسيتونين:
في ظل التوازن الطبيعي، تخضع مادة ما قبل البروكالسيتونين لعملية تصنيع أولية بواسطة خلايا الغدة الدرقية من النوع C. لاحقًا، يتحول هذا الببتيد إلى بروكالسيتونين عبر فصل تسلسل إشارة مكون من 25 حمضًا أمينيًا بواسطة الإندوببتيدازات. ويتكون الناتج النهائي، الكالسيتونين، وهو هرمون مكون من 32 حمضًا أمينيًا مسؤول عن تنظيم مستوى الكالسيوم في الدم، بعد تحويله بواسطة إنزيم محول البروهرمون. [9] عادةً، تؤدي الظروف الفسيولوجية إلى مستويات منخفضة جدًا من البروكالسيتونين في الدم، تقل عن 0.05 نانوغرام/مل. مع ذلك، يمكن أن يزداد تصنيع البروكالسيتونين بمقدار 100 إلى 1000 ضعف نتيجةً لوجود السموم الداخلية أو السيتوكينات المنتشرة في الدم، مثل إنترلوكين-6، وعامل نخر الورم ألفا، وإنترلوكين-1 بيتا، والتي تؤثر على أنسجة مختلفة. [10]
يحدث تصنيع البروكالسيتونين خارج الغدة الدرقية في الكبد والبنكرياس والكلى والرئة والأمعاء وكريات الدم البيضاء؛ ومن الجدير بالذكر أن تصنيع البروكالسيتونين يثبط داخل هذه الأنسجة في غياب العدوى البكتيرية. [11] في المقابل، تؤدي السيتوكينات التي تُفرز عقب العدوى الفيروسية، مثل إنترفيرون غاما، إلى انخفاض مستوى البروكالسيتونين، مما يُبرز ميزة أخرى لاختبارات البروكالسيتونين. [12]

متطلبات العينة والإجراءات لفحص و تحليل البروكالسيتونين:
يمكن استخدام عينات مصل الدم أو البلازما البشرية لتحديد مستوى البروكالسيتونين (PCT). وللحصول على نتائج دقيقة، يجب أن تكون عينات المصل والبلازما خالية من الفيبرين وخلايا الدم الحمراء وأي جسيمات أخرى. [13] قد تحتوي عينات المصل من المرضى الذين يتلقون علاجًا مضادًا للتخثر أو مذيبًا للجلطات على الفيبرين نتيجة عدم اكتمال تكوين الجلطة. [14] لا يُنصح باستخدام العينات المُعطَّلة حراريًا، أو العينات المُجمَّعة، أو العينات المُتحلِّلة بشكل واضح، أو العينات التي تحتوي على تلوث ميكروبي واضح، أو العينات التي ينمو عليها فطريات. يُوصى باستخدام البلازما للحصول على نتائج سريعة. [15]
يجب أن تكون عينات اختبار البروكالسيتونين خالية من الفقاعات. أزل الفقاعات باستخدام عود التطبيق قبل التحليل. استخدم عود تطبيق جديد لكل عينة لمنع التلوث المتبادل. لضمان اتساق النتائج، أعد تدوير العينات بالطرد المركزي قبل الاختبار إذا كانت تحتوي على الفيبرين أو خلايا الدم الحمراء أو أي مواد جسيمية أخرى. [16] أظهرت عينات بلازما ومصل الدم المعالجة بمادة EDTA والمخزنة مجمدة عند درجة حرارة -70 درجة مئوية أو أقل استقرارًا لمدة تصل إلى 18 شهرًا. [17]
الاختبارات التشخيصية:
الحركية
أظهرت الدراسات أن مستويات البروكالسيتونين (PCT) في الدم ترتفع بعد 6 إلى 12 ساعة من الإصابة الأولية بالعدوى البكتيرية، وتستمر في الارتفاع تدريجيًا خلال الساعتين إلى الأربع ساعات التالية لبدء الإنتان. [18] [10] يبلغ نصف عمر البروكالسيتونين ما بين 20 إلى 24 ساعة؛ لذا، عند وجود استجابة مناعية مناسبة من المضيف وتلقي العلاج بالمضادات الحيوية، تنخفض مستويات البروكالسيتونين بنسبة 50% خلال 24 ساعة. [11]
التحليلات الكيميائية
في الممارسة السريرية الحالية، طُوِّرت عدة فحوصات كيميائية للكشف عن مستويات البروكالسيتونين في مصل الدم بحساسيات متفاوتة، حيث تُظهر معظمها حساسية وظيفية تبلغ حوالي 0.06 نانوغرام/مل. [3] كان أحد أوائل الفحوصات المتاحة تجاريًا فحصًا مناعيًا متجانسًا يستخدم تقنية انبعاث الكريبتات المُضخَّمة والمُعتمدة على الزمن. [12] يتكون هذا الفحص من جسم مضاد متعدد النسائل من الأغنام ضد الكالسيتونين، وجسم مضاد أحادي النسيلة ضد الكاتاكالسين، يرتبط بتسلسل الأحماض الأمينية للكالسيتونين والكاتاكالسين في البروكالسيتونين عبر طريقة الساندويتش. يستخدم الفحص من 20 إلى 50 مل من البلازما أو المصل، ويستغرق 19 دقيقة لإتمامه؛ وعادةً ما تُحصل النتائج في غضون ساعة واحدة من سحب المصل. [19]
إجراءات اختبار تحليل البروكالسيتونين:
تعتمد جميع طرق التحليل المتاحة حاليًا لتحديد كمية البروكالسيتونين (PCT) على تقنيات المقايسة المناعية. [13] تُستخدم تقنية المقايسة المناعية للجسيمات الدقيقة المتألقة كيميائيًا (CMIA) لتحديد كمية البروكالسيتونين في مصل وبلازما الدم البشري. [20] تُخلط العينات مع جسيمات دقيقة مغناطيسية مغلفة بأجسام مضادة للبروكالسيتونين، ثم تُحضن. يرتبط البروكالسيتونين الموجود في العينة بالجسيمات الدقيقة المغلفة بالأجسام المضادة. يُغسل المزيج، ثم يُضاف مُقترن الأكريدينيوم المُوسوم بالأجسام المضادة للبروكالسيتونين لتكوين مزيج التفاعل، ويُحضن المزيج. بعد دورة الغسل، تُضاف محاليل ما قبل التحفيز والتحفيز. [21] يُقاس التفاعل الكيميائي الضوئي الناتج بوحدات الضوء النسبية (RLUs). توجد علاقة طردية بين كمية البروكالسيتونين في العينة ووحدات الضوء النسبية التي يكشفها النظام البصري. [20]
يتوفر اختبار سريع لقياس مستوى البروكالسيتونين (PCT) باستخدام تقنية الكروماتوغرافيا المناعية. يظهر شريط ملون على شريط الاختبار بعد 30 دقيقة من وضع 200 ميكرولتر من المصل أو البلازما؛ وتُقاس شدة الشريط بمقارنتها ببطاقة مرجعية. تُعرض النتائج كالتالي: أقل من 0.5، من 0.5 إلى 2.0، من 2.0 إلى 10، وأكثر من 10 ميكروغرام/لتر. [22] مع ذلك، قد تحد الطبيعة شبه الكمية لهذه النتائج من استخدامها السريري عندما يكون تغير مستوى البروكالسيتونين مهمًا لمراقبة الحالة السريرية للمريض. قد يظل هذا الاختبار مفيدًا عندما لا تتوفر قياسات كمية خلال فترة زمنية معقولة، مثل ساعة إلى ثلاث ساعات. [23]
العوامل المتداخلة في تحليل البروكالسيتونين:
على الرغم من أن فحوصات البروكالسيتونين (PCT) قد أظهرت نتائج واعدة على مر السنين، إلا أن هناك العديد من القيود التي لا تزال تستدعي النظر قبل تطبيق هذه الاختبارات في الممارسة السريرية اليومية. [13] على سبيل المثال، ثبت أن مستويات البروكالسيتونين في الدم قد ترتفع أيضًا في حالات غير معدية، مثل الصدمات، والحروق، وبعض أنواع السرطان (سرطان الخلايا النخاعية من النوع C، وسرطان الرئة ذو الخلايا الصغيرة، والسرطانة القصبية)، والعلاج بمعدلات المناعة الذي يزيد من السيتوكينات الالتهابية، والصدمة القلبية، وخلال اليومين الأولين من العمر، وأثناء غسيل الكلى البريتوني، ولدى مرضى تليف الكبد، وخاصةً مرضى تليف الكبد من الفئة C حسب تصنيف تشايلد-بوغ. [4] علاوة على ذلك، قد ترتفع مستويات البروكالسيتونين بشكل خاطئ لدى المرضى الذين يعانون من درجات متفاوتة من مرض الكلى المزمن، مما قد يؤدي بدوره إلى تغيير النتائج الأساسية، ويجعل تحديد وجود عدوى بكتيرية كامنة أمرًا صعبًا. [24] لذلك، يحتاج الطبيب إلى استبعاد السيناريوهات المذكورة أعلاه لضمان عدم وجود عوامل أخرى قد تحجب قياسات البروكالسيتونين. [25]
قد يُظهر فحص البروكالسيتونين (PCT) تداخلاً عند جمع عينة من شخص يتناول مكملاً غذائياً يحتوي على جرعة عالية من البيوتين (المعروف أيضاً بفيتامين B7 أو B8، أو فيتامين H، أو الإنزيم المساعد R). [26] يُنصح بسؤال جميع المرضى الذين لديهم مؤشر لإجراء فحص البروكالسيتونين عن تناولهم لمكملات البيوتين. يجب تنبيه المرضى إلى التوقف عن تناول البيوتين لمدة 72 ساعة على الأقل قبل جمع العينة. [27] قد يحدث تأثير هوك عند التركيزات العالية جداً من البروكالسيتونين، مما يؤدي إلى انخفاض كبير في القيمة المُبلغ عنها. [28]
يجب أيضًا مراعاة فعالية تكلفة فحوصات البروكالسيتونين، إذ يؤدي الإفراط في استخدامها في أقسام الطوارئ إلى تكاليف إضافية. يبلغ متوسط سعر الفحص حوالي 9.44 دولارًا أمريكيًا، وهو سعر زهيد نسبيًا. مع ذلك، لا يشمل هذا السعر المبالغ التي تغطيها شركات التأمين، ولا تكاليف الحصول على العينات. [29] اكتشف ساليناس وزملاؤه أنه من بين 142,644 فحصًا للبروكالسيتونين أُجريت خلال عام واحد، كان من الممكن تجنب 44.1% منها بناءً على الحالة السريرية والنتائج، مما كان سيوفر 594,390 دولارًا أمريكيًا سنويًا. [30]
في بيئة العناية المركزة، أجرى كيب وزملاؤه تجربة عشوائية مضبوطة لتحديد فعالية اختبارات البروكالسيتونين (PCT) من حيث التكلفة لدى مرضى الإنتان. وخلصوا إلى أن هذه الاختبارات حسّنت معدلات الوفيات وقللت من مدة العلاج بالمضادات الحيوية. مع ذلك، وجدوا أن متوسط تكلفة المرضى الذين خضعوا لاختبارات البروكالسيتونين كان أعلى بمقدار 2704 دولارًا أمريكيًا من تكلفة المرضى الذين لم يخضعوا لها. [31] لذا، ينبغي على الأطباء توخي الحذر عند طلب اختبارات البروكالسيتونين لضمان ممارسة طبية فعالة من حيث التكلفة. [29]
النتائج، والتقارير، والاستنتاجات الهامة
يبلغ نصف عمر البروكالسيتونين (PCT) من 20 إلى 24 ساعة، مما يوفر للأطباء والباحثين جدولًا زمنيًا تقريبيًا لبدء انخفاض مستوياته بعد السيطرة الفسيولوجية على العدوى الجهازية. عند الوصول إلى هذه السيطرة، ينخفض مستوى البروكالسيتونين بنسبة 50% تقريبًا خلال 24 ساعة. [10] تستخدم الممارسة السريرية الحالية مستويات قطع مختلفة للبروكالسيتونين لتحديد بدء العلاج بالمضادات الحيوية وإيقافه. يلعب السياق السريري والظروف المحيطة دورًا أساسيًا في تحديد مستوى القطع المناسب. مع ذلك، أظهرت معظم الأبحاث أن مستويات البروكالسيتونين ذات دلالة سريرية في نطاق 0.1 إلى 0.5 نانوغرام/مل. [11] كما أظهرت الأبحاث أن مستويات البروكالسيتونين الأقل من 0.1 نانوغرام/مل تتمتع بقيمة تنبؤية سلبية عالية (96.3%) لاستبعاد العدوى البكتيرية. [3]
استخدمت السيناريوهات السريرية التالية مستويات قطع مختلفة من PCT لتحديد مصدر العملية المعدية وكذلك متى يمكن استخدام العلاج بالمضادات الحيوية أو إيقافه: [11]
التهاب المفاصل وتحليل البروكالسيتونين:
- مستوى القطع لـ PCT: من 0.1 إلى 0.25 نانوغرام/مل
- دور اختبار البروكالسيتونين: التمييز بين التهاب المفاصل المعدي (الإنتاني) والتهاب المفاصل غير المعدي.
- نوع الدراسة: دراسة رصدية
العدوى البكتيرية في الدم وتحليل البروكالسيتونين:
- مستوى القطع لـ PCT: 0.25 نانوغرام/مل
- دور اختبار البروكالسيتونين: استبعاد العدوى الجرثومية في الدم.
- نوع الدراسة: دراسة رصدية
عدوى مجرى الدم (الأولية)
- مستوى القطع لـ PCT: 0.1 نانوغرام/مل
- دور اختبار البروكالسيتونين: التمييز بين العدوى الحقيقية والعينة الملوثة.
- نوع الدراسة: دراسة رصدية
تفاقم التهاب الشعب الهوائية الحاد / مرض الانسداد الرئوي المزمن:
- مستوى القطع لـ PCT: من 0.1 إلى 0.5 نانوغرام/مل
- دور العلاج بالمضادات الحيوية: تقليل التعرض (غير الضروري) للمضادات الحيوية في قسم الطوارئ وفي بيئة المرضى الداخليين دون حدوث نتائج سلبية.
- نوع الدراسة: تجربة عشوائية مضبوطة
التهاب الشغاف المعدي
- مستوى القطع لـ PCT: 2.3 نانوغرام/مل
- دور اختبار البروكالسيتونين: دقة تشخيصية عالية للتنبؤ بالتهاب الشغاف الحاد.
- نوع الدراسة: دراسة رصدية
التهاب السحايا:
- مستوى القطع لـ PCT: 0.5 نانوغرام/مل
- دور اختبار البروكالسيتونين: التمييز بين التهاب السحايا الفيروسي والتهاب السحايا البكتيري وتقليل التعرض للمضادات الحيوية.
- نوع الدراسة: قبل وبعد
قلة العدلات:
- مستوى القطع لـ PCT: من 0.1 إلى 0.5 نانوغرام/مل
- دور اختبار البروكالسيتونين: تحديد العدوى البكتيرية الجهازية لدى المرضى الذين يعانون من نقص العدلات.
- نوع الدراسة: دراسة رصدية
الالتهاب الرئوي و تحليل البروكالسيتونين:
- مستوى القطع لـ PCT: من 0.1 إلى 0.5 نانوغرام/مل
- دور العلاج بالمضادات الحيوية: تقليل التعرض للمضادات الحيوية أثناء الإقامة في المستشفى دون حدوث آثار سلبية.
الحمى بعد العملية الجراحية:
- مستوى القطع لـ PCT: من 0.1 إلى 0.5 نانوغرام/مل
- دور اختبار البروكالسيتونين: التمييز بين العدوى بعد العمليات الجراحية والحمى غير المعدية.
- نوع الدراسة: دراسة رصدية
العدوى بعد العمليات الجراحية
- مستوى القطع لـ PCT: من 0.5 إلى 1.0 نانوغرام/مل
- دور العلاج بالمضادات الحيوية: تقليل استخدام المضادات الحيوية في بيئات العناية المركزة الجراحية دون حدوث نتائج ضارة.
- نوع الدراسة: تجربة عشوائية مضبوطة
تسمم الدم الحاد مع أو بدون صدمة
- مستوى القطع لـ PCT: من 0.25 إلى 0.5 نانوغرام/مل
- دور اختبار البروكالسيتونين: الحد من استخدام المضادات الحيوية في وحدات العناية المركزة دون حدوث نتائج ضارة.
- نوع الدراسة: تجربة عشوائية مضبوطة
التهابات الجهاز التنفسي العلوي
- مستوى القطع لـ PCT: من 0.1 إلى 0.25 نانوغرام/مل
- دور اختبار البروكالسيتونين: الحد من استخدام المضادات الحيوية في وحدات العناية المركزة دون حدوث نتائج ضارة.
- نوع الدراسة: تجربة عشوائية مضبوطة
التهابات المسالك البولية
- مستوى القطع لـ PCT: 0.25 نانوغرام/مل
- دور اختبار البروكالسيتونين: تحديد مدى إصابة الكلى.
- نوع الدراسة: دراسة رصدية
الالتهاب الرئوي المرتبط بجهاز التنفس الصناعي
- مستوى القطع لـ PCT: من 0.1 إلى 0.25 نانوغرام/مل
- دور العلاج بالمضادات الحيوية: تقليل استخدام المضادات الحيوية دون حدوث نتائج ضارة.
- نوع الدراسة: تجربة عشوائية مضبوطة
بمجرد تحديد المستوى الحرج، ينبغي تحديد توقيت وعدد مرات قياس البروكالسيتونين (PCT) لتقييم كفاية مكافحة العدوى. [32] تشير البيانات السريرية الحالية إلى ضرورة إعادة قياس مستويات البروكالسيتونين في مصل الدم بعد 6 إلى 24 ساعة، في حال عدم وجود دليل على تحسن سريري تلقائي، مثل زوال عدم استقرار الدورة الدموية. بعد بدء العلاج بالمضادات الحيوية، يُوصى بتقييم قيم البروكالسيتونين كل يوم إلى يومين لضمان تغطية كافية. علاوة على ذلك، ينبغي إيقاف دورات المضادات الحيوية بمجرد انخفاض مستويات البروكالسيتونين إلى أقل من 0.1 نانوغرام/مل أو بنسبة 80 إلى 90% عن القياس الأولي. [11]
وُضعت خوارزميات خاصة بأقسام الطوارئ والعناية المركزة، تُتيح للأطباء طريقة سريعة لتحديد وقت بدء أو إيقاف المضادات الحيوية. [13] على سبيل المثال، وُضعت خوارزمية لتحديد وقت بدء العلاج بالمضادات الحيوية في قسم الطوارئ للمرضى المصابين بعدوى الجهاز التنفسي. [33] وتوصي الإرشادات باستخدام المضادات الحيوية عندما تكون مستويات البروكالسيتونين (PCT) أعلى من 0.25 نانوغرام/مل؛ ويجب إعادة قياس مستويات البروكالسيتونين في الأيام الثالث والخامس والسابع. ويجب إيقاف المضادات الحيوية عندما تنخفض مستويات البروكالسيتونين إلى أقل من 0.25 نانوغرام/مل أو تنخفض بنسبة 80 إلى 90%. إذا استمر ارتفاع مستوى البروكالسيتونين، فيُرجى النظر في خيارات علاجية أخرى. [11]
في وحدة العناية المركزة، تم تطبيق خوارزمية لتحديد متى يجب إيقاف العلاج بالمضادات الحيوية لدى مرضى الإنتان. [34] توصي الخوارزمية بإيقاف المضادات الحيوية عندما تنخفض مستويات البروكالسيتونين (PCT) إلى أقل من 0.5 نانوغرام/مل أو تنخفض بنسبة 80% عن أعلى قيمة لها. مع ذلك، إذا ظلت مستويات البروكالسيتونين مرتفعة (أكثر من 0.5 نانوغرام/مل)، يُنصح بمواصلة العلاج بالمضادات الحيوية أو تغيير العلاج بالكامل. [11] وقد استُخدمت هذه الخوارزميات بنجاح في التجارب السريرية، وأثبتت فعاليتها في تقليل الاستخدام الإجمالي للمضادات الحيوية، وبالتالي تحسين إدارة استخدامها. مع ذلك، هناك حاجة إلى مزيد من البحث لضمان إمكانية تكرار هذه النتائج بشكل كافٍ على نطاق أوسع، وذلك من خلال إجراء المزيد من التجارب السريرية بدلاً من الدراسات الرصدية. [35]
الأهمية السريرية:
من الثابت علميًا أن التشخيص المبكر للعدوى البكتيرية يُسهم في خفض معدلات الوفيات والإصابة بالأمراض بين جميع المرضى. [36] كما أن التشخيص الفعال للعدوى البكتيرية يُتيح للأطباء بدء العلاج بالمضادات الحيوية عند الحاجة، مما يمنع سوء استخدامها والإفراط في استخدامها. ومع استمرار تزايد مقاومة المضادات الحيوية، بات من الضروري للأطباء تحديد خوارزميات وفحوصات مخبرية مختلفة تُساعد في الحفاظ على معايير استخدام المضادات الحيوية الحالية. [37]
لسوء الحظ، تفتقر معظم الفحوصات الأولية لتشخيص العدوى، مثل زراعة الدم وبروتين سي التفاعلي، إلى الكفاءة والدقة اللازمتين لعلاج المرضى على الفور. لذلك، طُوِّرت فحوصات مصل البروكالسيتونين (PCT) لتزويد مقدمي الرعاية الصحية بطريقة كشف مبكرة لتحديد مصدر الاستجابة الالتهابية الجهازية (مثلًا، بكتيرية أو غير بكتيرية). ويحد الكشف المبكر بدوره من تطور مقاومة المضادات الحيوية، ويقلل من تعرض المرضى لها عندما لا تعود هناك حاجة إليها. [11]
أظهرت القيمة التنبؤية لـ PCT أهمية سريرية، إذ تُوفر للأطباء ارتباطًا إيجابيًا بين شدة المرض وارتفاع مستويات PCT في الدم، لا سيما لدى مرضى الإنتان. [12] ورغم أن فحوصات PCT أظهرت نتائج واعدة، إلا أن جدواها الاقتصادية لا تزال محل نقاش. وقد أظهرت الأبحاث الحالية أن هذه الفحوصات تُستخدم بإفراط لعدم وجود إرشادات كافية تحدد متى يجب إجراؤها ومتى يجب تجنبها. [30] لذا، ثمة حاجة إلى مزيد من البحث المعمق حول الأهمية السريرية لهذه الفحوصات على نطاق واسع ومن خلال تجارب سريرية عشوائية، لوضع إرشادات تضمن ممارسة الطب بكفاءة اقتصادية. [31]
مراقبة الجودة والسلامة المختبرية:
بالنسبة للاختبارات غير المعفاة، تشترط لوائح المختبرات، كحد أدنى، تحليل مستويين على الأقل من مواد التحكم مرة كل 24 ساعة. ويمكن للمختبرات، عند الضرورة، تحليل عينات مراقبة الجودة بشكل متكرر لضمان دقة النتائج. وينبغي تحليل عينات مراقبة الجودة بعد معايرة أو صيانة جهاز التحليل للتحقق من صحة أداء الطريقة. [38] ولتقليل مراقبة الجودة عند إجراء اختبارات تقل فيها توصيات الشركات المصنعة عن تلك التي تشترطها الهيئة التنظيمية (مثل مرة واحدة شهريًا)، يمكن للمختبرات وضع خطة فردية لمراقبة الجودة (IQCP) تتضمن إجراء تقييم للمخاطر المتعلقة بمصادر الخطأ المحتملة في جميع مراحل الاختبار، ووضع خطة لمراقبة الجودة للحد من احتمالية حدوث الأخطاء. [39] وتُستخدم قواعد ويستغارد المتعددة لتقييم عمليات مراقبة الجودة. وفي حالة مخالفة أي قاعدة، يجب اتخاذ الإجراءات التصحيحية والوقائية المناسبة قبل إجراء الاختبار على المرضى. [40]
يجب على المختبر المشاركة في برنامج مراقبة الجودة الخارجية أو اختبار الكفاءة (PT) لأنه شرط تنظيمي صادر عن مراكز خدمات الرعاية الطبية والخدمات الطبية (CMS) ضمن لوائح تعديلات تحسين المختبرات السريرية (CLIA). يُسهم ذلك في ضمان دقة وموثوقية المختبر مقارنةً بالمختبرات الأخرى التي تُجري نفس التحاليل أو تحاليل مماثلة. [41] تُراقب مراكز خدمات الرعاية الطبية والخدمات الطبية (CMS) وهيئات الاعتماد التطوعية المشاركة الإلزامية والنتائج المُسجلة. ينبغي إدراج خطة اختبار الكفاءة كجزء من خطة تقييم الجودة (QA) وبرنامج الجودة الشامل للمختبر. [42]
اعتبر جميع العينات ومواد التحكم ومواد المعايرة معدية محتملة. اتخذ الاحتياطات المعتادة اللازمة للتعامل مع جميع كواشف المختبر. يجب التخلص من جميع النفايات وفقًا للإرشادات المحلية. ارتدِ قفازات ومعطف المختبر ونظارات واقية عند التعامل مع عينات دم الإنسان. ضع جميع رؤوس الأنابيب البلاستيكية وأكواب العينات والقفازات التي تلامس الدم في حاوية النفايات البيولوجية الخطرة. [43] تخلص من جميع الأواني الزجاجية ذات الاستخدام الواحد في حاويات النفايات الحادة. غطِّ جميع أسطح العمل بورق ماص للأسطح ذي الاستخدام الواحد، وتخلص منه في حاويات النفايات البيولوجية الخطرة أسبوعيًا أو عند حدوث تلوث بالدم. امسح جميع أسطح العمل أسبوعيًا. [44]
تحسين نتائج فرق الرعاية الصحية:
مع استمرار تزايد مقاومة البكتيريا للأدوية في جميع أنحاء العالم، بات من الضروري للغاية تعزيز الاستخدام الرشيد للمضادات الحيوية. [37] يوفر البروكالسيتونين (PCT) لمقدمي الرعاية الصحية مؤشرًا أكثر دقة لتحديد وجود العدوى البكتيرية مقارنةً بالأساليب الحالية. لذا، يمكن استخدام فحوصات البروكالسيتونين لتحديد ما إذا كان من الضروري بدء العلاج بالمضادات الحيوية أو إيقافه أو تغييره بناءً على تغير مستوياته في الدم، مما يقلل من الاستخدام الكلي أو سوء استخدام المضادات الحيوية. [4] علاوة على ذلك، أثبتت هذه الفحوصات فائدتها كمؤشر تنبؤي للمرضى في وحدات العناية المركزة. مع ذلك، لا تزال هناك حاجة إلى مزيد من البحث لتحديد مدى ملاءمة فحوصات البروكالسيتونين لهذا الغرض. [11]
تُستخدم فحوصات البروكالسيتونين (PCT) في العديد من الحالات السريرية؛ وتشير الأبحاث الحالية إلى أن مستويات البروكالسيتونين تكون أكثر فائدة في حالات التفاقم الحاد لمرض الانسداد الرئوي المزمن (COPD) لتحديد متى وكيف يجب البدء بالعلاج بالمضادات الحيوية. [11] تنص الإرشادات الحالية للجمعية الأوروبية لأمراض الجهاز التنفسي والجمعية الأمريكية لأمراض الصدر على أن استخدام المضادات الحيوية في حالات تفاقم مرض الانسداد الرئوي المزمن أمرٌ مثير للجدل، نظرًا لعدم كفاية الأبحاث التي تُظهر تحسنًا في النتائج السريرية. لذلك، توصي هذه الإرشادات بإجراء المزيد من دراسات الفعالية واستخدام المؤشرات الحيوية لتحديد متى يكون استخدام المضادات الحيوية مناسبًا سريريًا. [45] يمكن استخدام مؤشر حيوي، مثل البروكالسيتونين، لتحديد ما إذا كانت المضادات الحيوية مناسبة في حالات التفاقم الحاد لمرض الانسداد الرئوي المزمن؛ مما يُحسّن من إدارة استخدام المضادات الحيوية ويقلل من المضاعفات المرتبطة بالاستخدام غير الضروري للمضادات الحيوية. [37]
بشكل عام، تُعدّ مستويات البروكالسيتونين (PCT) مؤشراً مخبرياً واعداً لتشخيص العدوى البكتيرية. مع ذلك، فإنّ فائدة هذا الاختبار محدودة بحسب البيئة السريرية وفئة المرضى. لذا، يجب إجراء المزيد من البحوث قبل تطبيق إرشادات اختبار البروكالسيتونين في الممارسة السريرية اليومية.
آخر تحديث: 06/05/2026
المصادر:
References
- 1.
- Le Moullec JM, Jullienne A, Chenais J, Lasmoles F, Guliana JM, Milhaud G, Moukhtar MS. The complete sequence of human preprocalcitonin. FEBS Lett. 1984 Feb 13;167(1):93-7. [PubMed]
- 2.
- Assicot M, Gendrel D, Carsin H, Raymond J, Guilbaud J, Bohuon C. High serum procalcitonin concentrations in patients with sepsis and infection. Lancet. 1993 Feb 27;341(8844):515-8. [PMC free article] [PubMed]
- 3.
- Riedel S, Melendez JH, An AT, Rosenbaum JE, Zenilman JM. Procalcitonin as a marker for the detection of bacteremia and sepsis in the emergency department. Am J Clin Pathol. 2011 Feb;135(2):182-9. [PubMed]
- 4.
- Hatzistilianou M. Diagnostic and prognostic role of procalcitonin in infections. ScientificWorldJournal. 2010 Oct 01;10:1941-6. [PMC free article] [PubMed]
- 5.
- Katz SE, Sartori LF, Williams DJ. Clinical Progress Note: Procalcitonin in the Management of Pediatric Lower Respiratory Tract Infection. J Hosp Med. 2019 Nov 01;14(11):688-690. [PMC free article] [PubMed]
- 6.
- Creamer AW, Kent AE, Albur M. Procalcitonin in respiratory disease: use as a biomarker for diagnosis and guiding antibiotic therapy. Breathe (Sheff). 2019 Dec;15(4):296-304. [PMC free article] [PubMed]
- 7.
- Hochreiter M, Köhler T, Schweiger AM, Keck FS, Bein B, von Spiegel T, Schroeder S. Procalcitonin to guide duration of antibiotic therapy in intensive care patients: a randomized prospective controlled trial. Crit Care. 2009;13(3):R83. [PMC free article] [PubMed]
- 8.
- Schuetz P, Wirz Y, Sager R, Christ-Crain M, Stolz D, Tamm M, Bouadma L, Luyt CE, Wolff M, Chastre J, Tubach F, Kristoffersen KB, Burkhardt O, Welte T, Schroeder S, Nobre V, Wei L, Bucher HC, Bhatnagar N, Annane D, Reinhart K, Branche A, Damas P, Nijsten M, de Lange DW, Deliberato RO, Lima SS, Maravić-Stojković V, Verduri A, Cao B, Shehabi Y, Beishuizen A, Jensen JS, Corti C, Van Oers JA, Falsey AR, de Jong E, Oliveira CF, Beghe B, Briel M, Mueller B. Procalcitonin to initiate or discontinue antibiotics in acute respiratory tract infections. Cochrane Database Syst Rev. 2017 Oct 12;10(10):CD007498. [PMC free article] [PubMed]
- 9.
- Duan S, Gu X, Fan G, Zhou F, Zhu G, Cao B. C-reactive protein or procalcitonin combined with rhinorrhea for discrimination of viral from bacterial infections in hospitalized adults in non-intensive care units with lower respiratory tract infections. BMC Pulm Med. 2021 Sep 28;21(1):308. [PMC free article] [PubMed]
- 10.
- Lippi G, Sanchis-Gomar F. Procalcitonin in inflammatory bowel disease: Drawbacks and opportunities. World J Gastroenterol. 2017 Dec 21;23(47):8283-8290. [PMC free article] [PubMed]
- 11.
- Schuetz P, Albrich W, Mueller B. Procalcitonin for diagnosis of infection and guide to antibiotic decisions: past, present and future. BMC Med. 2011 Sep 22;9:107. [PMC free article] [PubMed]
- 12.
- Christ-Crain M, Müller B. Biomarkers in respiratory tract infections: diagnostic guides to antibiotic prescription, prognostic markers and mediators. Eur Respir J. 2007 Sep;30(3):556-73. [PubMed]
- 13.
- Samsudin I, Vasikaran SD. Clinical Utility and Measurement of Procalcitonin. Clin Biochem Rev. 2017 Apr;38(2):59-68. [PMC free article] [PubMed]
- 14.
- Weglöhner W, Struck J, Fischer-Schulz C, Morgenthaler NG, Otto A, Bohuon C, Bergmann A. Isolation and characterization of serum procalcitonin from patients with sepsis. Peptides. 2001 Dec;22(12):2099-103. [PubMed]
- 15.
- Sheng H, Zhang X, Peng Z, Chen F. The Effects of Different Blood Sample Types on Quantitative Detection of Procalcitonin. Clin Lab. 2022 Feb 01;68(2) [PubMed]
- 16.
- Magnette A, Chatelain M, Chatelain B, Ten Cate H, Mullier F. Pre-analytical issues in the haemostasis laboratory: guidance for the clinical laboratories. Thromb J. 2016;14:49. [PMC free article] [PubMed]
- 17.
- Ikeda K, Ichihara K, Hashiguchi T, Hidaka Y, Kang D, Maekawa M, Matsumoto H, Matsushita K, Okubo S, Tsuchiya T, Furuta K., Committee for Standardization, The Japanese Society of Laboratory Medicine (JSLM). Evaluation of the short-term stability of specimens for clinical laboratory testing. Biopreserv Biobank. 2015 Apr;13(2):135-43. [PubMed]
- 18.
- Becker KL, Nylén ES, White JC, Müller B, Snider RH. Clinical review 167: Procalcitonin and the calcitonin gene family of peptides in inflammation, infection, and sepsis: a journey from calcitonin back to its precursors. J Clin Endocrinol Metab. 2004 Apr;89(4):1512-25. [PubMed]
- 19.
- Meisner M. Pathobiochemistry and clinical use of procalcitonin. Clin Chim Acta. 2002 Sep;323(1-2):17-29. [PubMed]
- 20.
- Hubl W, Krassler J, Zingler C, Pertschy A, Hentschel J, Gerhards-Reich C, Mack M, Demant T. Evaluation of a fully automated procalcitonin chemiluminescence immunoassay. Clin Lab. 2003;49(7-8):319-27. [PubMed]
- 21.
- Carcamo Yañez VA, Göpfert JC, Otto M, Tumani H, Peter A, Joos TO. Development and Validation of an Ultrasensitive Procalcitonin Sandwich Immunoassay. High Throughput. 2017 Nov 16;6(4) [PMC free article] [PubMed]
- 22.
- Waterfield T, Maney JA, Lyttle MD, McKenna JP, Roland D, Corr M, Patenall B, Shields MD, Woolfall K, Fairley D., Paediatric Emergency Research in the UK and Ireland (PERUKI). Diagnostic test accuracy of point-of-care procalcitonin to diagnose serious bacterial infections in children. BMC Pediatr. 2020 Oct 21;20(1):487. [PMC free article] [PubMed]
- 23.
- Waterfield T, Maney JA, Hanna M, Fairley D, Shields MD. Point-of-care testing for procalcitonin in identifying bacterial infections in young infants: a diagnostic accuracy study. BMC Pediatr. 2018 Dec 12;18(1):387. [PMC free article] [PubMed]
- 24.
- Wu SC, Liang CX, Zhang YL, Hu WP. Elevated serum procalcitonin level in patients with chronic kidney disease without infection: A case-control study. J Clin Lab Anal. 2020 Feb;34(2):e23065. [PMC free article] [PubMed]
- 25.
- Grace E, Turner RM. Use of procalcitonin in patients with various degrees of chronic kidney disease including renal replacement therapy. Clin Infect Dis. 2014 Dec 15;59(12):1761-7. [PubMed]
- 26.
- Rodrigo J, Bullock H, Mumma BE, Kasapic D, Tran N. The prevalence of elevated biotin in patient cohorts presenting for routine endocrinology, sepsis, and infectious disease testing. Clin Biochem. 2022 Jan;99:118-121. [PubMed]
- 27.
- Öncül Ü, Eminoğlu FT, Köse E, Doğan Ö, Özsu E, Aycan Z. Serum biotin interference: A troublemaker in hormone immunoassays. Clin Biochem. 2022 Jan;99:97-102. [PubMed]
- 28.
- Fernando SA, Wilson GS. Multiple epitope interactions in the two-step sandwich immunoassay. J Immunol Methods. 1992 Jul 06;151(1-2):67-86. [PubMed]
- 29.
- Westwood M, Ramaekers B, Whiting P, Tomini F, Joore M, Armstrong N, Ryder S, Stirk L, Severens J, Kleijnen J. Procalcitonin testing to guide antibiotic therapy for the treatment of sepsis in intensive care settings and for suspected bacterial infection in emergency department settings: a systematic review and cost-effectiveness analysis. Health Technol Assess. 2015 Nov;19(96):v-xxv, 1-236. [PMC free article] [PubMed]
- 30.
- Salinas M, López-Garrigós M, Flores E, Uris J, Leiva-Salinas C., Pilot Group of the Appropriate Utilization of Laboratory Tests (REDCONLAB) working group. Procalcitonin in the Emergency Department: A potential expensive over-request that can be modulated through institutional protocols. Am J Emerg Med. 2018 Jan;36(1):158-160. [PubMed]
- 31.
- Kip MMA, van Oers JA, Shajiei A, Beishuizen A, Berghuis AMS, Girbes AR, de Jong E, de Lange DW, Nijsten MWN, IJzerman MJ, Koffijberg H, Kusters R. Cost-effectiveness of procalcitonin testing to guide antibiotic treatment duration in critically ill patients: results from a randomised controlled multicentre trial in the Netherlands. Crit Care. 2018 Nov 13;22(1):293. [PMC free article] [PubMed]
- 32.
- Mat Nor MB, Md Ralib A. Procalcitonin clearance for early prediction of survival in critically ill patients with severe sepsis. Crit Care Res Pract. 2014;2014:819034. [PMC free article] [PubMed]
- 33.
- Schuetz P, Briel M, Christ-Crain M, Stolz D, Bouadma L, Wolff M, Luyt CE, Chastre J, Tubach F, Kristoffersen KB, Wei L, Burkhardt O, Welte T, Schroeder S, Nobre V, Tamm M, Bhatnagar N, Bucher HC, Mueller B. Procalcitonin to guide initiation and duration of antibiotic treatment in acute respiratory infections: an individual patient data meta-analysis. Clin Infect Dis. 2012 Sep;55(5):651-62. [PMC free article] [PubMed]
- 34.
- Kip MM, Kusters R, IJzerman MJ, Steuten LM. A PCT algorithm for discontinuation of antibiotic therapy is a cost-effective way to reduce antibiotic exposure in adult intensive care patients with sepsis. J Med Econ. 2015;18(11):944-53. [PubMed]
- 35.
- Rhee C. Using Procalcitonin to Guide Antibiotic Therapy. Open Forum Infect Dis. 2017 Winter;4(1):ofw249. [PMC free article] [PubMed]
- 36.
- Kovacs A, Leaf HL, Simberkoff MS. Bacterial infections. Med Clin North Am. 1997 Mar;81(2):319-43. [PubMed]
- 37.
- Livorsi DJ, Nair R, Lund BC, Alexander B, Beck BF, Goto M, Ohl M, Vaughan-Sarrazin MS, Goetz MB, Perencevich EN. Antibiotic Stewardship Implementation and Antibiotic Use at Hospitals With and Without On-site Infectious Disease Specialists. Clin Infect Dis. 2021 May 18;72(10):1810-1817. [PubMed]
- 38.
- Kinns H, Pitkin S, Housley D, Freedman DB. Internal quality control: best practice. J Clin Pathol. 2013 Dec;66(12):1027-32. [PubMed]
- 39.
- Westgard JO. Internal quality control: planning and implementation strategies. Ann Clin Biochem. 2003 Nov;40(Pt 6):593-611. [PubMed]
- 40.
- Schoenmakers CH, Naus AJ, Vermeer HJ, van Loon D, Steen G. Practical application of Sigma Metrics QC procedures in clinical chemistry. Clin Chem Lab Med. 2011 Nov;49(11):1837-43. [PubMed]
- 41.
- 42.
- Joint Commission on Accreditation of Healthcare Organizations. Accepted: Revised laboratory proficiency testing requirement. Jt Comm Perspect. 2011 Apr;31(4):4. [PubMed]
- 43.
- Rojo-Molinero E, Alados JC, de la Pedrosa EG, Leiva J, Pérez JL. [Safety in the Microbiology laboratory]. Enferm Infecc Microbiol Clin. 2015 Jun-Jul;33(6):404-10. [PubMed]
- 44.
- 45.
- Wedzicha JA, Miravitlles M, Hurst JR, Calverley PM, Albert RK, Anzueto A, Criner GJ, Papi A, Rabe KF, Rigau D, Sliwinski P, Tonia T, Vestbo J, Wilson KC, Krishnan JA. Management of COPD exacerbations: a European Respiratory Society/American Thoracic Society guideline. Eur Respir J. 2017 Mar;49(3) [PubMed]