علاج الثلاسيميا الجديد
علاج الثلاسيميا الجديد بالجينات أو دواء زينتيجلو zynteglo, العلاج الجذري النهائي للثلاسيميا بيتا, هل يوجد علاج جديد للثلاسيميا؟ هل يمكن الشفاء من مرض ثلاسيميا؟ ما هو العلاج الجيني او بالجينات لمرضى الثلاسيميا؟ افضل علاج لمرض الثلاسيميا؟
زينتيغلو هو علاج جيني يُعطى لمرة واحدة لعلاج الثلاسيميا بيتا (المعروفة أيضًا باسم الثلاسيميا بيتا الكبرى أو فقر دم كولي) لدى المرضى الذين يحتاجون إلى عمليات نقل دم منتظمة. تنتج الثلاسيميا بيتا عن طفرة في جين بيتا غلوبين، مما يؤدي إلى انخفاض إنتاج الجسم لبيتا غلوبين أو انعدامه. يُصنع زينتيغلو خصيصًا لكل مريض، باستخدام خلاياه الجذعية الدموية، ويُضاف إليه نسخ وظيفية من جين بيتا غلوبين. قد يُتيح ذلك للمريض إنتاج كمية كافية من الهيموغلوبين، مما يُغنيه عن الحاجة إلى عمليات نقل الدم المنتظمة.
ماذا لو استطعت التخلي عن عمليات نقل الدم؟
ZYNTEGLO ™ هو علاج جيني معتمد من إدارة الغذاء والدواء الأمريكية، ولديه القدرة على تحرير الأشخاص المصابين بمرض الثلاسيميا بيتا من عمليات نقل الدم المنتظمة.
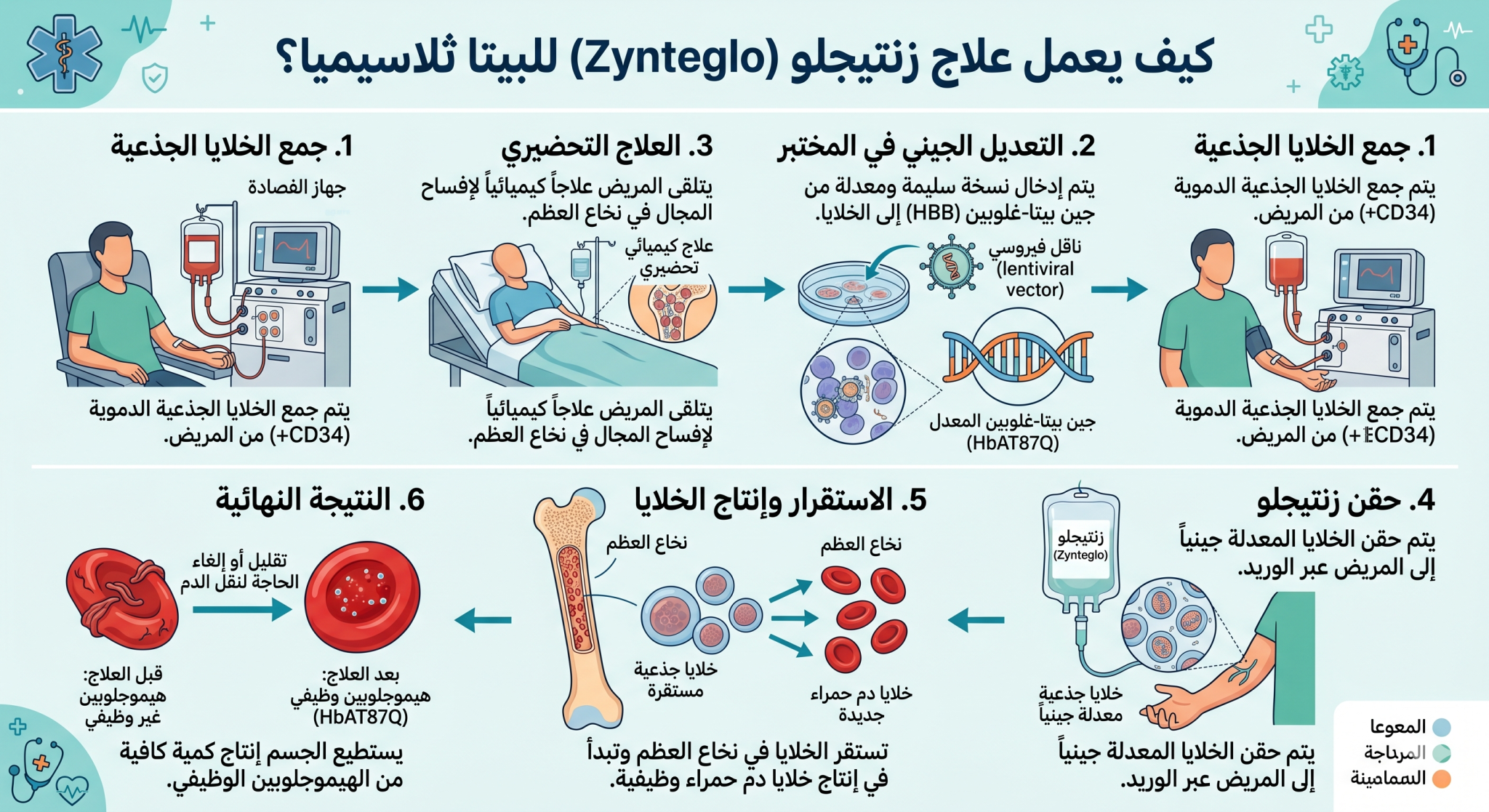
كيف يتم تحضير دواء زينتيجلو zynteglo؟
يتم جمع الخلايا الجذعية للدم من جسمك
- تم تصنيع ZYNTEGLO خصيصاً لك باستخدام خلاياك الخاصة
- بمجرد جمع خلايا الدم الجذعية، يتم إرسالها إلى المختبر لبدء عملية التصنيع
يتم تصنيع ZYNTEGLO عن طريق إضافة نسخ عاملة من جين بيتا غلوبين إلى الخلايا التي تم جمعها
-
- تتم إضافة الجين العامل إلى خلايا الدم الجذعية التي تم جمعها بمساعدة ناقل من خارج جسمك
تُعاد خلاياك الجذعية المعدلة (ZYNTEGLO) إلى جسمك عن طريق الحقن الوريدي.
- تنتقل الخلايا الجذعية للدم عبر مجرى الدم إلى نخاع العظم
- ثم تقوم هذه الخلايا الجذعية الدموية بإنتاج خلايا جذعية دموية جديدة في عملية تسمى الانغراس.
وفي النهاية في جسم المريض يتم إنتاج خلايا الدم الحمراء الجديدة التي تحتوي على الهيموجلوبين البالغ الوظيفي.
ملخص عن مرض الثلاسيميا:
الثلاسيميا بيتا، المعروفة أيضًا باسم الثلاسيميا بيتا الكبرى أو فقر دم كولي، هي اضطراب وراثي يؤثر على إنتاج الهيموجلوبين، مما يؤدي إلى فقر الدم (نقص خلايا الدم الحمراء). يحتاج الأطفال المصابون بهذه الحالة إلى عمليات نقل دم متكررة لاستعادة مستويات خلايا الدم الحمراء الطبيعية وتخفيف الأعراض. مع ذلك، تحتوي عمليات نقل الدم على الحديد الذي قد يُسبب مضاعفات طويلة الأمد، بما في ذلك ارتفاع مستويات الحديد في الأعضاء، مما يؤدي إلى تلف الكبد والقلب والبنكرياس وغيرها من الأعضاء. يُعدّ زينتيغلو™ (بيتي بيغلوجين أوتوتيمسيل) علاجًا جينيًا معتمدًا من إدارة الغذاء والدواء الأمريكية ، يُقدّم الأمل للعائلات من خلال إعفاءهم من الحاجة إلى عمليات نقل الدم المنتظمة. يفخر معهد السرطان وأمراض الدم في مستشفى لوس أنجلوس للأطفال بكونه أحد المراكز القليلة على الساحل الغربي التي تُقدّم زينتيغلو للمرضى الأطفال المصابين بالثلاسيميا بيتا المعتمدة على نقل الدم.

ما هو العلاج الجيني زينتيغلو؟
زينتيغلو هو علاج جيني يُعطى لمرة واحدة، مُصمم للأطفال من عمر 4 سنوات فما فوق المصابين بمرض الثلاسيميا بيتا المعتمد على نقل الدم . يساعد نقل الدم في السيطرة على المرض وتخفيف بعض أعراضه، بينما يستهدف زينتيغلو السبب الكامن وراء المرض على المستوى الجيني. فهو يُساعد الجسم على إنتاج الهيموغلوبين الوظيفي، مما يُقلل أو حتى يُلغي الحاجة إلى نقل الدم في المستقبل.
يستخدم زينتيغلو الخلايا الجذعية الدموية الخاصة بطفلك لعلاج الثلاسيميا الكبرى. تتضمن عملية العلاج النموذجية الخطوات التالية:
- الخلايا الجذعية خلايا مميزة للغاية، فهي أساس جهاز المناعة بأكمله، وتساهم في تكوين خلايا الدم الحمراء. تعيش هذه الخلايا في المادة الإسفنجية داخل العظام، والتي تُسمى نخاع العظم، وبعضها ينتشر في مجرى الدم.
- يبدأ العلاج بدواء يساعد على نقل المزيد من الخلايا الجذعية من نخاع العظم إلى مجرى الدم، وهذا ما يسمى بالتعبئة.
- ثم يتم جمع الخلايا الجذعية الدموية من المريض من خلال قسطرة يتم وضعها في الوريد مما يسمح بإزالة الخلايا الجذعية عن طريق إجراء يسمى فصل مكونات الدم.
- بعد جمع الخلايا الجذعية، يتم إرسالها إلى المصنع حيث يتم تعديل الخلايا في المختبر عن طريق إضافة نسخ وظيفية من جين بيتا غلوبين الذي يصنع الهيموغلوبين باستخدام ناقل فيروسي (فيروس غير مسبب للأمراض) يسمى ناقل الفيروسات البطيئة (LVV).
- ثم يُعطى المريض العلاج الكيميائي لتفريغ نخاع العظم، مما يوفر مساحة لاستقبال الخلايا المعدلة. ويُسمى هذا نظام التكييف.
- بمجرد أن تصبح الخلايا المعدلة جاهزةً وتكتمل عملية التكييف، تُعاد الخلايا الجذعية المعدلة الخاصة بالمريض إلى الجسم عبر حقنة وريدية واحدة، تمامًا كما في عملية نقل الدم، ولكن باستخدام خلايا جذعية معدلة جديدة. تتجه هذه الخلايا عائدةً إلى نخاع العظم وتبدأ في إنتاج خلايا دم حمراء جديدة تحتوي على الهيموجلوبين الطبيعي.
من خلال استهداف السبب الكامن وراء المرض، يمتلك دواء زينتيغلو القدرة على تحرير المرضى من عمليات نقل الدم المتكررة، وتحسين الصحة العامة، وتعزيز نوعية حياتهم.
كيف يختلف علاج زينتيغلو عن العلاجات الأخرى؟
يُعدّ نقل الدم بانتظام علاجًا شائعًا لمرضى الثلاسيميا الكبرى، حيث يُزوّد الجسم بخلايا دم حمراء إضافية. إلا أن هذه العمليات تنطوي على خطر تراكم الحديد الزائد في الجسم، وهو ما يُعرف بفرط الحديد. وقد يُسبب ذلك مضاعفات في أعضاء حيوية، كالقلب والجهاز الهرموني والكبد. ويتطلب ضبط مستويات الحديد علاجًا مستمرًا بالاستخلاب لإزالة الحديد الزائد، وهو ما قد يُشكّل صعوبة على الأطفال وعائلاتهم.
يمكن لزراعة نخاع العظم أن تشفي من الثلاسيميا الكبرى، لكنها تتطلب متبرعًا مطابقًا تمامًا. حتى مع استخدام متبرع مطابق تمامًا، كالأخ أو الأخت، توجد مخاطر عديدة. من أبرز هذه المخاطر داء الطعم ضد المضيف (GVHD)، وهو حالة تتعرف فيها خلايا المتبرع على جسم المريض على أنه مختلف وتهاجمه. لا يحدث هذا دائمًا، لكنه قد يكون خطيرًا. قد يكون الأخ أو الأخت هو الأنسب، لكن احتمالية تطابق نخاع العظم بين شقيقين لا تتجاوز ربع الاحتمال، مما يحدّ بشكل كبير من إمكانية الحصول على عملية الزرع.
هناك ثلاث مزايا رئيسية للعلاج الجيني للأطفال المصابين بالثلاسيميا المنقولة بالدم. الميزة الأكبر هي أن هذا النهج يقضي على خطر الإصابة بداء الطعم حيال المضيف. ثانيًا، المريض هو المتبرع، لذا يمكنه الخضوع لهذا العلاج الجيني بمجرد بلوغه سن الرابعة. أخيرًا، يُعدّ دواء زينتيغلو علاجًا يُعطى لمرة واحدة، ويُلغي أو يُقلل بشكل كبير من الحاجة إلى عمليات نقل الدم المنتظمة، وبالتالي يُبطئ من تفاقم تراكم الحديد في الجسم.
يُعدّ مستشفى لوس أنجلوس للأطفال (CHLA) رائدًا على المستوى الوطني في أبحاث وعلاجات الخلايا والجينات لدى الأطفال. بالإضافة إلى علاج زينتيغلو، نوفر خيارًا علاجيًا جينيًا ثانيًا لعلاج الثلاسيميا المعتمدة على نقل الدم (TDT) يُسمى كاسجيفي . على عكس زينتيغلو الذي يستخدم ناقلًا فيروسيًا لإيصال جين مُعدّل، يستخدم كاسجيفي تقنية كريسبر لتحرير الجينات لتعديل الحمض النووي للطفل لإنتاج هيموجلوبين جنيني. يُمكن لكلا العلاجين الاستغناء عن عمليات نقل الدم المتكررة من خلال إنتاج خلايا دم حمراء وظيفية، مما يُقلل من خطر تراكم الحديد الزائد، وتلف الأعضاء، والمضاعفات الأخرى المرتبطة بنقل الدم.
لماذا قد يحتاج طفلك إلى زينتيغلو؟
إذا تم تشخيص إصابة طفلك (4 سنوات فأكثر) بمرض الثلاسيميا بيتا ويحتاج إلى عمليات نقل دم منتظمة، فإن علاج زينتيغلو يوفر حلاً طويل الأمد وراحةً فعّالة. من خلال معالجة السبب الجيني للمرض، يسمح هذا العلاج الجيني الرائد للجسم بإنتاج الهيموغلوبين الوظيفي الخاص به، مما يلغي أو يقلل بشكل ملحوظ الحاجة إلى عمليات نقل الدم. يمنح زينتيغلو الأطفال المؤهلين فرصة تقليل زياراتهم للمستشفى وتحسين جودة حياتهم.
فوائد ومخاطر دواء زينتيغلو:
فوائد:
بالنسبة للأطفال المصابين بمرض الثلاسيميا بيتا المعتمد على نقل الدم، يمكن أن يوفر العلاج الجيني Zynteglo أكثر من مجرد تخفيف الأعراض، بل يمكنه أيضًا أن يمنحهم مستقبلًا أفضل.
- الاستقلال عن نقل الدم: يمكّن زينتيغلو الجسم من إنتاج خلايا الدم الحمراء الصحية الخاصة به، ويزيل أو يقلل بشكل ملحوظ الحاجة إلى عمليات نقل الدم المنتظمة.
- انخفاض مخاطر الحديد: يتم التخلص من المضاعفات الشائعة الناتجة عن عمليات نقل الدم المنتظمة، مثل زيادة الحديد، والحاجة إلى العلاج بالاستخلاب بمجرد إزالة الحديد المتبقي.
- جودة حياة أفضل: فبدون الحاجة إلى عمليات نقل الدم المتكررة وعلاج استخلاب الحديد، يمكن للأطفال التركيز على المدرسة والأنشطة والاستمتاع بطفولتهم.
- فوائد طويلة الأمد: في التجارب السريرية، تمكن 89% من الأفراد الذين تلقوا زينتيغلو من التوقف عن عمليات نقل الدم بعد حوالي أربعة أسابيع من العلاج، وكان لديهم مستويات طبيعية من الهيموجلوبين لعدة سنوات بعد العلاج.
المخاطر المحتملة والآثار الجانبية:
كما هو الحال مع أي علاج طبي، توجد مخاطر وآثار جانبية محتملة عند تلقي العلاج الجيني بتقنية زينتيغلو. ترتبط معظم هذه المخاطر بعملية الزرع نفسها، وتزول عندما تنمو الخلايا الجديدة بشكل جيد ويعود الجهاز المناعي إلى وضعه الطبيعي.
- انخفاض عدد خلايا الدم: قد يؤدي انخفاض مستوى الصفائح الدموية إلى النزيف، كما أن انخفاض مستوى خلايا الدم البيضاء قد يزيد من خطر الإصابة بالعدوى. ويمكن أن يحدث هذا بعد العلاج لمدة تصل إلى ستة أشهر.
- العدوى: نظرًا لأن العلاج الكيميائي يضعف جهاز المناعة، فهناك احتمال متزايد للإصابة بالعدوى حتى تتعافى المناعة تمامًا.
- الآثار الجانبية المؤقتة: يمكن أن يسبب العلاج الكيميائي وانخفاض تعداد الدم الحمى والغثيان وآلام البطن التي تستمر حتى يتم تكوين خلايا الدم الجديدة (من أسبوعين إلى أربعة أسابيع تقريبًا).
- المتابعة طويلة الأمد: هناك احتمال ضئيل للإصابة بسرطان الدم بعد تلقي علاج زينتيغلو، لذا يلزم إجراء فحوصات دورية لمدة لا تقل عن 15 عامًا. على الرغم من وجود هذا الاحتمال، لم تُسجّل أي حالات في التجارب السريرية حتى الآن.
من هم المؤهلون لتلقي علاج زينتيغلو؟
سيساعدك أخصائيونا في تحديد ما إذا كان علاج زينتيغلو هو العلاج المناسب لطفلك، وذلك باستخدام الاختبارات الجينية، وتحاليل الدم، والفحوصات الصحية الشاملة. قد يكون طفلك مؤهلاً لتلقي علاج زينتيغلو إذا:
- تم تشخيص إصابتهم بمرض الثلاسيميا بيتا، أو فقر الدم كولي، ويخضعون لعمليات نقل دم منتظمة.
- يجب ألا يقل عمرهم عن 4 سنوات وقت العلاج
- إنهم يستوفون متطلبات الفحص الصحي والجيني المحددة.
حتى لو لم يكن طفلك مؤهلاً، يمكننا مساعدتك في توجيهك إلى خيارات علاجية أخرى.
في مستشفى لوس أنجلوس للأطفال، نتبع نهجًا متعدد التخصصات لضمان أفضل النتائج الممكنة.
الاستعداد للعلاج
يتم اتخاذ عدة خطوات لضمان استعداد طفلك للعلاج.
- قد يخضع طفلك لاختبارات جينية للتأكد من أهليته. نحن من بين المستشفيات القليلة المتخصصة في طب الأطفال التي تقدم اختبارات جينية داخلية من خلال مركزنا للطب الشخصي .
- قبل جمع الخلايا الجذعية ومعالجتها، من المهم أن يستوفي طفلك متطلبات صحية محددة. سيتم إجراء فحوصات الدم وتقييم وظائف الأعضاء وفحص العدوى لضمان سلامة طفلك.
- سيجتمع معك أخصائيونا لمناقشة خطة العلاج، والإجابة على أي أسئلة قد تكون لديك، وإعدادك أنت وطفلك للخطوات التالية.
- يجب الحفاظ على مستوى الهيموجلوبين عند مستوى محدد قبل بدء العلاج، لذلك ستكون هناك حاجة إلى استمرار عمليات نقل الدم.
- سيتم استخدام قسطرة وريدية مركزية (خط مركزي) لتسهيل خطوات متعددة خلال العلاج.
أثناء العلاج:
يتم جمع الخلايا الجذعية عادةً في مركز الحقن التابع لنا ، يليه العلاج في وحدة زراعة نخاع العظم للمرضى الداخليين، مع مراقبة دقيقة من قبل فريقنا المتخصص. يُعد برنامج زراعة نخاع العظم أحد أكبر برامج زراعة نخاع العظم للأطفال من نوعه في العالم، وهو معتمد من قبل مؤسسة اعتماد العلاج الخلوي (FACT).
- لمساعدتك أنت وطفلك على الاستعداد للعلاج، يتوفر أخصائي رعاية الأطفال لتقديم الدعم طوال فترة العلاج وأثناء إقامتك في المستشفى. بإمكانه شرح كل خطوة بلغة مناسبة لعمر طفلك. يتمثل دوره في المساعدة على تخفيف التوتر والقلق، وتلبية الاحتياجات الطبية والعاطفية والنفسية التي قد تكون لديك أنت وطفلك.
- تبدأ العملية بتناول عوامل النمو وأدوية تحفيز الخلايا الجذعية لمدة تتراوح بين خمسة وسبعة أيام. تعمل هذه الأدوية على زيادة إنتاج الخلايا الجذعية ونقلها من نخاع العظم إلى مجرى الدم لجمعها. ثم يتم جمع الخلايا الجذعية على مدى ثلاثة أيام تقريبًا. تُجرى هذه العملية بالكامل في مركزنا المتخصص بالحقن الوريدي للمرضى الخارجيين.
- تُجمع الخلايا الجذعية باستخدام عملية تُسمى فصل مكونات الدم، حيث يُسحب الدم، ويُفصل مكون محدد منه، ثم يُعاد الدم المتبقي إلى الجسم. تُجرى عملية فصل مكونات الدم في مركز الحقن الوريدي التابع لنا.
- تُرسل هذه الخلايا الجذعية بعد ذلك إلى مختبر متخصص لإجراء تعديل جيني عليها، حيث يُضاف إليها جين بيتا غلوبين وظيفي. قد تستغرق هذه العملية من شهرين إلى ثلاثة أشهر. خلال هذه الفترة، قد يكون الحفاظ على الخصوبة خيارًا متاحًا قبل بدء العلاج الكيميائي التحضيري. ستستشيرين طبيب طفلك.
- بمجرد أن تصبح الخلايا المعدلة جاهزة، سيتم إدخال طفلك إلى مستشفانا لبدء العلاج الكيميائي التحضيري. يُعطى هذا العلاج في وحدة زراعة نخاع العظم للمرضى الداخليين، حيث يعمل على إزالة خلايا نخاع العظم القديمة لإفساح المجال للخلايا الجديدة المعدلة. قد تشمل الآثار الجانبية المؤقتة التعب والغثيان وانخفاض تعداد الدم.
- بعد اكتمال العلاج الكيميائي التحضيري، تُعاد الخلايا إلى دم طفلك عبر حقنة وريدية في وحدة زراعة نخاع العظم. ستنتقل هذه الخلايا المعدلة وراثيًا إلى نخاع العظم وتبدأ بإنتاج خلايا دم حمراء سليمة. عادةً، يبقى طفلك في وحدة زراعة نخاع العظم لمدة تتراوح بين أربعة وثمانية أسابيع حتى يحدث الالتصاق، وهي المرحلة التي تبدأ فيها الخلايا الجذعية المزروعة بالنمو بشكل جيد وإنتاج كمية كافية من خلايا الدم السليمة.
الرعاية اللاحقة والتعافي:
- بعد العلاج، سيخضع طفلك لمراقبة دقيقة من قبل فريقنا في المستشفى لمدة تتراوح بين أربعة إلى ثمانية أسابيع تقريباً لرصد أي ردود فعل ولضمان سلامته.
- سيخضعون لفحوصات دم منتظمة للتحقق من مستويات الصفائح الدموية وخلايا الدم البيضاء.
- بعد العلاج، ستكون مناعة طفلك ضعيفة أثناء تعافي جهازه المناعي. نتخذ إجراءات إضافية للوقاية من العدوى، وقد ينصح طبيبك بتأجيل التطعيمات لفترة من الوقت.
- سيواصل فريقنا مراقبة صحة طفلك بشكل عام وتقدمه من خلال زيارات متابعة منتظمة، وخاصة خلال السنة الأولى بعد العلاج.
- يوصى بمراقبة طفلك من قبل فريقنا مرة واحدة على الأقل سنوياً لمدة لا تقل عن 15 عاماً، وذلك بسبب المخاطر المحتملة للإصابة بسرطان الدم.
ستتلقى إرشادات من فرق أمراض الدم والعلاج الجيني لدينا لتحديد مواعيد زيارات العيادة والرعاية المنزلية.
الآثار الجانبية لدواء زينتيجلو zynteglo:
معلومات السلامة الهامة
ما هي أهم المعلومات التي يجب أن أعرفها عن زينتيغلو؟
أكثر الآثار الجانبية شيوعاً لدواء زينتيغلو هي:
- في يوم العلاج باستخدام زينتيغلو
- زيادة معدل ضربات القلب
- ألم في البطن
- بعد العلاج لمدة تصل إلى 6 أشهر
- انخفاض مستوى الصفائح الدموية، مما قد يقلل من قدرة الدم على التجلط وقد يسبب النزيف
- انخفاض مستوى خلايا الدم البيضاء، مما قد يجعلك أكثر عرضة للإصابة بالعدوى.
- ألم في الذراعين أو الساقين
اتصل بمقدم الرعاية الصحية الخاص بك على الفور إذا كنت تعاني من نزيف جديد أو غير معتاد قد يشمل أيًا من هذه العلامات أو الأعراض:
- صداع شديد
- كدمات غير طبيعية
- نزيف الأنف
- وجود دم في البول أو البراز أو القيء
- يسعل دماً
- ألم غير معتاد في المعدة أو الظهر
قد تُعاني من آثار جانبية مرتبطة بأدوية أخرى تُعطى كجزء من نظام علاج زينتيغلو. استشر طبيبك بشأن هذه الآثار الجانبية المحتملة. قد يصف لك مقدمو الرعاية الصحية أدوية أخرى لعلاج هذه الآثار.
من المهم أن تخضع للمتابعة الطبية سنوياً لمدة لا تقل عن 15 عاماً لرصد أي تغيرات في دمك. يوجد احتمال للإصابة بسرطان الدم مرتبط بهذا العلاج؛ ومع ذلك، لم تُسجّل أي حالات في الدراسات التي أُجريت على دواء زينتيغلو. في حال تشخيص إصابتك بالسرطان، يُرجى من طبيبك المعالج التواصل مع شركة بلو بيرد بيو على الرقم 1-833-999-6378 .
كيف سأحصل على زينتيجلو؟
سيصف لك مقدمو الرعاية الصحية أدوية أخرى، بما في ذلك أدوية العلاج الكيميائي، كجزء من علاجك بدواء زينتيغلو. من المهم التحدث مع مقدم الرعاية الصحية حول مخاطر وفوائد جميع الأدوية المستخدمة في علاجك.
بعد الخضوع للعلاج الكيميائي، قد لا يكون من الممكن الحمل أو الإنجاب. لذا، يُنصح بمناقشة خيارات الحفاظ على الخصوبة مع الطبيب قبل بدء العلاج.
الخطوة الأولى: يُصنع دواء زينتيغلو خصيصاً لك من خلاياك الجذعية الدموية. سيقوم مقدم الرعاية الصحية الخاص بك بجمع خلاياك الجذعية الدموية من خلال عملية تُسمى التعبئة والفصل. تستغرق هذه العملية حوالي أسبوع واحد وقد تحتاج إلى التكرار.
يتم أيضًا جمع خلايا جذعية احتياطية (أو خلايا إنقاذ) وتخزينها في المستشفى. هذا إجراء احترازي في حال حدوث أي مشكلة أثناء العلاج. في هذه الحالة، ستُعاد إليك خلاياك الجذعية الاحتياطية. إذا تلقيت خلايا احتياطية، فلن تستفيد من علاج زينتيغلو.
الخطوة الثانية: سيتم إرسال خلاياك الجذعية من الدم إلى موقع التصنيع حيث تُستخدم في إنتاج دواء زينتيغلو. يستغرق الأمر ما يقارب 70-90 يومًا من وقت جمع خلاياك حتى يتم تصنيع زينتيغلو واختباره قبل شحنه إلى مقدم الرعاية الصحية الخاص بك، ولكن قد يختلف هذا الوقت.
الخطوة الثالثة: قبل تلقيك دواء زينتيغلو، سيخضعك طبيبك للعلاج الكيميائي لبضعة أيام لإفساح المجال في نخاع العظم. سيتم إدخالك إلى المستشفى لهذه الخطوة، وستبقى هناك حتى بعد حقن زينتيغلو.
الخطوة الرابعة: يُعطى دواء زينتيغلو عن طريق التسريب الوريدي. قد تتلقى أكثر من كيس واحد من زينتيغلو. يتم تسريب كل كيس في غضون 30 دقيقة أو أقل.
بعد حقن دواء زينتيغلو، ستبقى في المستشفى لمدة تتراوح بين 3 و6 أسابيع تقريبًا ليتمكن فريق الرعاية الصحية من متابعة تعافيك عن كثب. سيحدد الطبيب المعالج موعد عودتك إلى المنزل.
ما الذي يجب عليّ تجنبه بعد استخدام زينتيغلو؟
- لا تتبرع بالدم أو الأعضاء أو الأنسجة أو الخلايا.
ما هي الآثار الجانبية الإضافية المحتملة أو المرجحة لدواء زينتيغلو؟
لن يُسبب دواء زينتيجلو الإصابة بفيروس نقص المناعة البشرية (HIV). قد يُؤدي العلاج بزينتيجلو إلى ظهور نتيجة إيجابية خاطئة في بعض اختبارات فيروس نقص المناعة البشرية التجارية. إذا كنت بحاجة إلى إجراء اختبار فيروس نقص المناعة البشرية، فتحدث مع مقدم الرعاية الصحية الخاص بك حول الاختبار المناسب.
هذه ليست كل الآثار الجانبية المحتملة لدواء زينتيغلو. استشر طبيبك للحصول على نصائح طبية بشأن الآثار الجانبية. نشجعك على الإبلاغ عن أي آثار جانبية سلبية للأدوية الموصوفة إلى إدارة الغذاء والدواء الأمريكية (FDA). تفضل بزيارة الموقع الإلكتروني www.fda.gov/medwatch .
معلومات عامة:
من المهم إجراء فحوصات دورية لدى طبيبك، بما في ذلك تحاليل الدم السنوية على الأقل، للكشف عن أي آثار جانبية وللتأكد من استمرار فعالية دواء زينتيغلو. تحدث مع طبيبك بشأن أي مخاوف لديك.
آخر تحديث: 13/05/2026 – المصدر: chla.org